|
|
| | 1 | 2 | 3 |
| 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 |
| 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| 25 | 26 | 27 | 28 | 29 | 30 | 31 |
|
| |
|
|
|
|
|
|
|
|
PD �ä����Թ�ѹ
�ͺ�س�ͧ�觺��͡��...
�Ź�������...����� / �Ҿ��ͺ ��ͺ goffymew / �굺��͡������������ ����� / �δ���͡ ������� /�ͤ ���� / ���觺��͡ Zairill /�Ҿ�ͤRainfall in August / ẹ��Banner..����ٹ ... oranuch_sri
��ҷ���Һ�ä����Դ�ҡ�ѹ������ ����Դ��ҡ����Ǵ����.. �������Ѻ�����պҧ���ҧ... ��. ���ҧ��������ѡ ���������ͤ�㹤�ͺ��������դ��繾���Թ�ѹ ���������������褹���� ���Ҵٻ���ѵԻ�ҡ���ҷӧҹ�繪�ҧ��Сͺö¹��ͧ����ѷ�˭��ҡ����˹�� �ǡ��ҧ��Сͺö���Ѻ��õ�ҧ��Թ�Ҵ���������ʹ�ѹ �ҡ������ѧ���ͻ��ѹ����.....��������˵�˹�觷��������������Ѻ

�Ҿ��Сͺ�ä����Թ�ѹ (PD) �� �.�. 1880
�ä����Թ�ѹ (PD) �������¡���� ��Ҿ���Թ�ѹ ���ä�ҧ�к�����ҷ������������ѧ����觼ŵ���к�����ҷ��ǹ��ҧ ���觼ŵ�ͷ���к���觡������к����� �ͧ��ҧ��� �ҡ�õ�ҧ� �ѡ�Ф���� ��ҡ��͡�� ���������ä���Թ� �ҡ������ ����������ǡѺ�к���觡�á�о�����¢�� �ҡ�÷���� ���� �ҡ����� ������Ǫ�� ��� ��зç����Ӻҡ ������¡����ѹ��Ҿ���Թ�ѹ �͡�ҡ��� �ä����Թ�ѹ�ѧ�Ҩ�Դ������ͧ������ ˡ��� ��лѭ�ҷҧ�Ե��л���ҷ �� ��ù��Ѻ�Դ���� �ä�Ե �������û�ǹ ���͡������¹�ŧ�ĵԡ�����������ء���
�ä����Թ�ѹ��ǹ�˭��Դ����ºѧ��ԭ ���ջѨ���ʹѺʹع�ҧ��С�÷�����Ѻ����к� ��Ҹ������Է�����ѡɳ��Ф���������ҷ�����Ť�ʫ���������������մ� �����ѧ�繺���dz��ͧ��ǹ��ҧ�����ⴾ��չ价�������ҷ�ҹ�������Ǣ�ͧ�Ѻ��äǺ�����������������Ѥ�� ���˵آͧ��õ�¢ͧ�������ѧ����繷��������Ѵ ������֧��������Ǣͧ��ſҫԹ٤�չ����պʹ������������ҷ �Ѩ��·����������� ���� ��䡷ҧ�ѹ�ء����������Ǵ���� ����֧�� �ſ����� �������С�˹�ҹ��
����ԹԨ�����ǹ�˭�������ѭ�ҳ����ҡ�� ����ѡ����Ǣ�ͧ�Ѻ���������� �¾���ҡ��õ�Ǩ�к�����ҷ �����ҡ�ö����Ҿ�ҧ���ᾷ�� �� MRI �ͧ��������ҹԹ��ʹѺʹع����ԹԨ����� �·�����ҡ��������Դ���㹼�����������ҡ���� 60 �� ���ջ���ҳ������ 1 ������Ѻ�š�з� 㹼���������ع��¡��� 50 �� ���¡����ä����Թ�ѹ�����������ҡ������
�ѧ������Ը��ѡ�ҷ���Һ��Ѵ ��С���ѡ�Ҩ����价���ú�����ҡ�� ����ѡ�����ͧ���ѡ����֧����� L-DOPA, �ҵ�ҹ MAO-B �����ҡ�е��ⴻ��չ ������ä���Թ� ������ҹ����ջ���Է���Ҿ����ŧ��С������Դ�Ţ�ҧ��§����ѧࡵ��ҡ���������Ǣͧ��������ͷ��Ǻ�������� �������С�ÿ�鹿���ҧ��ºҧ�ٻẺ���ʴ������繶֧����Է���Ҿ㹡�ú�����ҡ�� ��á�е����ͧ��ǹ�֡�١���������ͺ�����ҡ�÷ҧ�к����������Ƿ���ع�ç㹡óշ���������� ����ѡ�ҹ��§��硹�������Ѻ����ѡ���ҡ�÷���������Ǣ�ͧ�Ѻ���������� �� ��ù��Ѻ���ʹԷ��������������蹤� ���آ��������������§�Ѻ����
��è�ṡ������
�ä����Թ�ѹ����ö��ṡ�����������»����� �ѧ���仹��:
�ä����Թ�ѹ: �ä�������ͧ�к�����ҷẺ����˹�ҷ�����ҡ�êѴਹ ���� �ҡ��������Ǫ�� �ҡ����� �秷��� ��з�ҷҧ�����蹤�
�ä����Թ�ѹ�Դ����: �ä����������ء����Թ�Ѻ�ᵹ��� 乡�� ��з�����Դ�����á���ҧ�к�����ҷ���Ѻ���ҡ��� �� �ҡ�����á��������ҡ�á�������͵����ç�˹����鹻���ҷ
�ä����Թ�ѹ�ͧ: �Դ�ҡ�� ��õԴ���� ��������ä����к�����ҷ��ǹ��ҧ
�ä����Թ�ѹẺ�ӧҹ�Դ����: �����Դ���Ԣͧ�к����������Ƿ���Դ�ҡ�������¹�ŧ���� �͡�˹�ͨҡ����������ͧ�к�����ҷ���ͤ����Դ���Ԣͧ�к�ⴾ��չ����ԡ
� �� 2024 ��è�ṡ�������оԨ�óҨҡ�ҡ�� �����Ԩ��������价�������ҧ��鹰ҹ�ҧ����Է��
�ä����Թ�ѹ����ö��ṡ�������Ը� �� ������ҡ�þ���Թ�ѹ�ǡ (Parkinson-plus syndrome) ����֧�ä����Թ�ѹ�����Ѻ�ҡ������ �ä����Թ�ѹ�Ѵ����㹡�����ä����Դ�ҡ Lewy body ��ж�����ä����Դ�ҡ synucleinopathy �������֧������ͧ����������� Lewy body �ä���������������ǹ��� ����ҡ������ ��辺����¡��� �ä����Թ�ѹ�ҧ�ѹ�ء���������ҡ�ҧ����������ա�������Ǣͧ��ſ�-synuclein
�ҡ������ѭ�ҳ
�ҡ�÷��觺͡�֧�ҡ�è��觼ŵ���к����������� ���� �ҡ����� ���������Ǫ�� ������������ ��з�ҷҧ�����蹤� �ҡ������ �Ҩ�觼ŵ���к�����ҷ�ѵ��ѵ������к�����ҷ�Ѻ��������֡ ������ �ĵԡ��� �ٻẺ��ù��Ѻ ��С���Ѻ���
�ҡ�÷���������ǡѺ�����������Ҩ�Դ��鹡��ҡ������ǡѺ���������ǹҹ�֧ 20 �� �ҡ������ҹ������ �ҡ�÷�ͧ�١ �ҡ���٭���¡���Ѻ���� �ҡ�üԴ���Էҧ������ ����ҡ�üԴ���Ԣͧ�ĵԡ�����ù��ѺẺ REM �繵� �·���� �ҡ������ǡѺ���������� �� ��ҷҧ�����蹤���С���Թ�Դ���� �ѡ�л�ҡ����������ä���Թ�
�ҡ�÷ҧ�к����������� 4 ��С�ö�����ѭ�ҳ��ѡ��ä����Թ�ѹ ���� �ҡ����� ���������Ǫ�� �����秵�� ��Ф��������蹤��ͧ��ҷҧ ������¡����ѹ��Ҿ���Թ�ѹ ���ҧ�á��� �ҡ������ �������Ǣ�ͧ�Ѻ�к����������ǡ羺������蹡ѹ
�ҡ��������ѭ�ҳ����ѡ�Դ��鹺��·���ش ����Ҩ��ҡ����㹢�оѡ���͢����������µ��� ���դ�����������ҧ 4�6 ���õ�� (�ͺ����Թҷ�) �ҡ����蹢ͧ�ä����Թ�ѹ�ѡ�Դ��鹷����� ������ö�觼ŵ����ǹ���� �ͧ��ҧ��� �� �� ᢹ ��� ��������ջҡ���蹡ѹ �ҡ�ù���ѡ���¡��� "��á�����" ���������������Ǫ����й�����������ͨ�������������������ǧ��� ��觪ǹ���֡�֧�Ԥ��ü�Ե�Ҵ��������ؤ�á� �������ҡ����蹨����ѭ�ҳ����ѧࡵ��Ѵਹ����ش �辺��§����ҳ 70�90 �����繵�ͧ��������ҹ��
�ҡ��������Ǫ���ѡ������ѡɳз���Ӥѭ����ش�ͧ�ä����Թ�ѹ ����ѧ����ä����Թ�ѹẺ��軡�Դ��� Ժ�¶֧�����ҡ�Ӻҡ㹡���ҧἹ ���������� ��С�ô��Թ��ô�ҹ���������� �觼���������������������ŧ����������ԨٴŴŧ ����觼ŵ�͡�÷ӧҹẺ������ͧ��о�����ѹ �ѧ��� �֧ú�ǹ�Ԩ������Ш��ѹ �� ����觵�� ��û������ ��С���Һ��� ����������˹�ҷ������Ǣ�ͧ�Ѻ���������Ǫ�ҷ�����Դ�ѡɳС���ʴ��͡�ҧ��˹�ҷ��Ŵŧ ������¡��� "�˹�һԴ�ѧ" �������������
�ҡ��������ͷ�����¡����ҡ��������� "�ҡ�õ֧" ��ͤ�����ҹ�ҹ���������������ҧ����������ᢹ��Ẻ��ʫտ ����觼š�з���ͼ����¶֧ 89 �����繵� �ҡ�ù���ѡ�Դ�����ѧ�ҡ��������ҡ�������С��������Ǫ�ҷ���ҹ㴴�ҹ˹�����ͷ���ͧ��ҧ�ͧ��ҧ��� ����Ҩ������Դ�ҡ�ûǴ������������͢����������ä���Թ� ���֧�� 2024 �ѧ���Ѵਹ����ҡ������Դ�ҡ��кǹ��÷ҧ��ǡ���ʵ����Ѵਹ�����繡���ʴ��ҡ���Ӥѭ���� �ͧ�ä����Թ�ѹ
�ҡ�������蹤��ͧ��ҷҧ (PI) �ѡ�Դ����������ѧ�ͧ�ä �觼����������������ˡ��� ����ͧŧ�Ҥ�͡�д١�ѡ �觼�������������ҧ��������ŧ����դس�Ҿ���ԵŴŧ �ҡ�� PI �ѡ����ҡ�����������������ѡ�Դ��� 10�15 ����ѧ�ҡ����ԹԨ��¤����á ����������á��ѧ�ҡ��������ä �ҡ�� PI �Ҩ�觪��֧���о���Թ�ѹ���Դ���� �����Һҧ���觢������Ҩ�ѧ����ҧ�֧�ҡ����ѡ���ҡ�������С�� ���� �ҡ����� ���������Ǫ�� ����ҡ����� �� PI ���Ѻ�������Ѻ���ҧ���ҧ��ҧ������ҡ�÷����� �����Ҩ�����Һ��� �֧������Դ�ҡ��������ҧ �ҡ�ù�������Ѻ���������Ǫ������ҡ����� ������Դ����ԹẺ���Է�����ѡɳ��繡���ԹẺ������� � ��з�ҷҧ���仢�ҧ˹��
�ҡ�÷ҧ�к����������Ƿ������� � ���� ���§�ٴ���Ѵ�����º ��������ͷ������ ���ŧ �ҡ����ѧ����Ҩ�Դ��鹡��ҡ�÷������� � ���䡷ҧ�к�����ҷ����� ��д����˵ع�� �֧�Ҩ������§�Ѻ�ҡ����� � �� �֧�ѧ����Һ��Ѵ
�к�����ҷ�Ѻ��������֡
�������¹�ŧ�ͧ�к�����ҷ�Ѻ��������֡�Ҩ������������¹�ŧ�ͧ��������֡ �������֧����ҷ�Ѻ���蹷�躡���ͧ ����ͧ��繷��Դ���� �����纻Ǵ ����ҡ�ê� �ѭ�Ҵ�ҹ����ͧ�������ԧ��鹷���Ҩ�Դ�����й���������ҡ�Ӻҡ㹡�è����˹����С���Ѻ����ȷҧ�ͧ��鹷���Ҵ
�繷���Һ�ѹ������ä��鹻���ҷ��ǹ�����Դ���㹼����¾���Թ�ѹ�ҡ�֧ 55 �����繵� �������ä���������˵آͧ�ҡ�ê���Ф����纻Ǵ��ǹ�˭�㹾���Թ�ѹ �躷�ҷ�ͧ�ä���㹡�÷ç��������蹤���С�÷ӧҹ�ͧ��������ͺ����ͧ�ѧ����繷�����㨡ѹ�չѡ
�к�����ҷ�ѵ��ѵ�
�������¹�ŧ��к�����ҷ�ѵ��ѵԷ�����¡��� dysautonomia �ѡ����Ǣ�ͧ�Ѻ�ҡ�õ�ҧ� �� �����Դ���Ԣͧ�к��ҧ�Թ����� �����ѹ���Ե���������ء� �˧����͡�ҡ�Թ� ���͡��鹻�������������
�ѭ�ҷҧ�к��ҧ�Թ����� ���� �ҡ�÷�ͧ�١ ��âѺ��������дǡ ������ҧ�������ҡ�Թ� ��С�á��Ӻҡ (�����ҡ�֧ 82%) �����á������Դ�ҡ���С��Ӻҡ ���� ��âҴ��� ���зؾ����ҡ�� ���˹ѡŴ ��лʹ�ѡ�ʺ�ҡ������ѡ �ҡ�÷ҧ�к��ҧ�Թ����÷������Ҩ�ع�ç�ͷ��з��������֡���ʺ�� ���ѹ���µ���آ�Ҿ ��з�����èѴ����ä�դ����Ѻ�� �����Ҩ�����Ǣ�ͧ�ѹ ���䡷����Ѵ�ͧ�ҡ������ҹ���ѧ������繷���Һ��Ѵ
�����ѹ���Ե���������ء� ��� �����ѹ���ԵŴŧ���ҧ������ͧ���ҧ���� 20 mmHg ����Ѻ�����ԡ���� 10 mmHg ����Ѻ������ԡ��������ҷ��á��ѧ�ҡ¡��Ǣ��㹷�ҵç �������ö�������� 30�50 �����繵�ͧ�ó� �����ѹ���Ե����Ҩ�������������¹�ͧ���ʹ��ѧ�����з�������˹������Ŵŧ ������ͧ �觼�����Դ�ҡ���ֹ��� ����Ҩ���������㹷���ش ����Ҩ������纻���������ª��Ե��
�ҡ������ �������Ǣ�ͧ�Ѻ�к�����ҷ�ѵ��ѵ� ���� �˧����͡�ҡ�Թ� ���鹻������������� ������ö�Ҿ�ҧ��������
�ҡ�÷ҧ�Ե����ҷ��л���ҷ (NPS) �ѡ�Դ����������ҡ�üԴ������硹���仨��֧�ҡ�ú����ͧ�����ç ������� �����Դ����㹡���Ѻ��� ������ �ĵԡ��� ���ͤ����Դ ����Ҩú�ǹ�Ԩ������Ш��ѹ Ŵ�س�Ҿ���Ե ���������������§㹡������Ѻ����ѡ���ʶҹ��Һ�� �ҡ�úҧ���ҧ �� ���Ы���������Ф����Ե��ѧ�� �ѡ���ҡ�÷ҧ�к����������Ƿ���蹪Ѵ�ҹ�֧���»� ����Ҩ���ѭ�ҳ���֧��þѲ�Ңͧ�ä����Թ�ѹ 㹢�з���ҡ����ǹ�˭��ѡ�����ŧ������ä���Թ� ����Ԩ���к���Ҽ����·�����ҡ�÷ҧ�к����������Ƿ���ع�ç���Ҩ��դ�������§��� NPS �٧��� 㹷ҧ��Ѻ�ѹ NPS �Ҩ������ä����Թ�ѹ���ŧ��
���Ы��������� NPS ��辺���·���ش����Դ���㹼�������ͺ����˹�� �����ҡ�÷ҧ������������ТҴ�����آ ��о������㹼��˭ԧ ����ԹԨ����Ҩ�����ҡ ���ͧ�ҡ�ҡ�ë������Һҧ���ҧ �� ������Ҫ�ҷҧ�Ե��С��������� �ѭ�Ҵ�ҹ������ ���ͤ�����ҡ���������¹�ŧ ���ѡɳФ���¤�֧�Ѻ�ҡ�÷ҧ�Ե�Ǫ����Դ�ҡ�ä����Թ�ѹ ����Ҩ�觼�����Դ�����Դ��ҵ�ǵ�� ��觾��������ä����Թ�ѹ ���ҧ�á��� ������������ҵ�ǵ���ѧ��ӡ���㹻�Ъҡ÷����
�ҡ����������ѡɳ��蹤�ͤ�������·ҧ����������Դ���㹻���ҳ 46 �����繵�ͧ������ ����ԹԨ��·����ҡ���ͧ�ҡ�Ҩ�¡�������͡�ҡ�ҡ�ë���������
�ä�Ե��ѧ�� (AD) �Դ���㹻���ҳ 43 �����繵�ͧ������ �ä��辺���·���ش ���� �ä��蹵��˹� �ä�Ե��ѧ�ŷ���� ����ä�Ե��ѧ�ŷҧ�ѧ�� �繷���Һ�ѹ����Ҥ����Ե��ѧ�ŷ�����ҡ�âͧ�ä����Թ�ѹ���ŧ
�ä�Ե�ҡ�ä����Թ�ѹ (PDP) �Դ���㹻���ҳ 20 �����繵�ͧ��������л�Сͺ�����Ҿ�� �Ҿ�ǧ�� ��Ф������ͼԴ� �ä�������Ǣ�ͧ�Ѻ��ⴻ��չ������ѡ���ҡ�÷ҧ�к����������� ����纻��·���ع�ç �ѵ�ҡ�����ª��Ե �ĵԡ�����������آ�Ҿ���Ŵŧ ��С����Ҿѡ㹺�ҹ�ѡ����ҷ��ҹ��� �͡�ҡ��� �ä����ѧ����ѹ��Ѻ���Ы�����������Ҩ���ѭ�ҳ�觪������������ä��ͧ����������з���ع�ç ���ᵡ��ҧ�ҡ�ä�Ե�ٻẺ��� PDP �ѡ�����ҡ�÷ҧ����ҷ�����ʷ��Ѵਹ �Ҩ�Ѻ���Ѻ�ҡ�÷ҧ�Ե�Ǫ���� ��������ԹԨ��·����ҡ
�ä�Ǻ����ç��е�� (Impulse-control disorders ���� ICD) ����㹼����»���ҳ������ 19 ���㹺�Ժ��ͧ�ä PD �ä���Ѵ����㹡�����ҡ�äǺ����ç��е�� (compulse-by-syndrome) ��С�����ҡ�äǺ���ⴾ��չ�Դ���� (dopamine dysregulation syndrome ���� DDS) �������㹡�����ҡ�äǺ����ç��е����оĵԡ����ع�ѹ��ѹ��� (impulse-by-syndrome ���� ICB) �ä������ѡɳ��蹤�ͤǺ����ç��е�����ҡ��ФǺ����ç��е�����ҡ ����դ�������ѹ����ԧ�ǡ�Ѻ������ҡ�е��ⴾ��չ
�����Դ���ԷҧʵԻѭ��
�����Դ���ԷҧʵԻѭ���Ҩ�Դ������������������͡�����ԹԨ��� ��Ш������ҡ��鹵���������Ңͧ�ä �������������ͧ�ҧʵԻѭ����硹���仨��֧������ͧ�������ҡ�ä����Թ�ѹ����ع�ç �����ҡ�üԴ���Ԣͧ��÷ӧҹ�ͧ��ͧ ��������㹡�û����żŷҧʵԻѭ�Ҫ��ŧ ��С���Ѻ�����С�û���ҳ���ҷ��Դ����
��ù��Ѻ
�����Դ���Ԣͧ��ù��Ѻ���������ä����Թ�ѹ����觼ŵ�ͼ����»���ҳ�ͧ������� �����Դ��������ҹ������ ��ù�����Ѻ �ҡ�ç�ǧ�����ҡ�ҧ�ѹ�ҡ�Թ� (EDS) ������ҡ�â���������آ (RLS) �����Դ���Ԣͧ�ĵԡ�����ù��ѺẺ REM (RBD) ��С�����㨼Դ���Ԣ�й��Ѻ (SDB) ����Ҩ���ŧ��������� RBD �Ҩ��������ҡ�÷ҧ�к��������������������������»� �ҡ�âͧ���Ф���ᵡ��ҧ�ѹ� �����Ҽ������ä����Թ�ѹ��ǹ�˭���ըѧ��С�÷ӧҹ�ͧ��ҧ��·������¹�ŧ�㹺ҧ��ǧ�ͧ�ä����ء���
����
PD ����Ǣ�ͧ�Ѻ�����Դ���Ԣͧ���˹ѧ���ª�Դ �� ����秼��˹ѧ��Դ������� ���˹ѧ�ѡ�ʺ�ҡ��ѹ ���ԡ�´��繵��� ����ä���˹ѧ�ѡ�ʺ�ҡ��ѹ���Ѻ�������Ѻ������ҡ�á����������Ƿ��觪��֧�����Դ���Ԣͧ�к�����ҷ ����ʴ��������������ö��Ǩ�� PD �������§��ҡ�������¹�ŧ�ͧ��������ͻ���ҷ��ҹ�� ���ѧ����֧�����Դ���Ԣͧ�����������¹͡�к�����ҷ�ա����
���˵���лѨ�������§
� �� 2024 ���˵ؾ�鹰ҹ�ͧ PD �ѧ����繷���Һ��Ѵ ���ѹ��ɰҹ������Ѻ�Է�ԾŨҡ�������ѹ�������ҧ�Ѩ��·ҧ�ѹ�ء����������Ǵ��������ѡ ���ҧ�á��� �Ѩ�������§����Ӥѭ����ش������� �����غѵԡ�ó� 1 �����繵�㹼�����������ҡ���� 65 �� ��л���ҳ 4.3 �����繵�㹼�����������ҡ���� 85 �� ��ǹ��Сͺ�ҧ�ѹ�ء�����Сͺ���� SNCA, LRRK2 ��� PARK2 �繵� 㹢�з���������§�������Ǵ��������֧��������ʡѺ�Ҧ����ŧ��������˹ѡ ��ǧ���Ңͧ�Ѩ��¡���������Ҩ�觼ŵ�͡�ô��Թ����ͤ����ع�ç�ͧ���е�ҧ�: 46 ���ҧ�á��� ����չ��й�⤵Թ�ʴ��س���ѵ�㹡�û���ͧ�к�����ҷ �֧����Ŵ��������§�ͧ PD �� ����ҳ 85 �����繵�ͧ�������Դ����繤��駤��� ������¤����������ջ���ѵԤ�ͺ����
�ѹ�ء���
PD 㹤������·��᤺����ö�ͧ��������ä�ҧ�ѹ�ء��� �¤Ҵ��Ҥ�������ö㹡�ö��·ʹ�ҧ�ѹ�ء��������������ҧ 22 �֧ 40 �����繵�㹡�����ҵԾѹ����ҧ� ����ҳ 15 �����繵�ͧ������ԹԨ����ä�ջ���ѵԤ�ͺ���� ��� 5�10 �����繵��Ҩ�Դ�ҡ��á��¾ѹ���ͧ�չ����§���������Դ�ä �����ҡ���ա�á��¾ѹ�������ҹ����Ҩ���������ä����
� �� 2024 �ա���кص��������§�ҧ�ѹ�ء�������ҳ 90 ���� 78 ���˹觨��� �չ����§����Ӥѭ ���� SNCA, LRRK2 ��� VPS35 ����Ѻ��ö��·ʹ�ҧ�ѹ�ء���Ẻ����������ṹ�� ��� PRKN, PINK1 ��� DJ1 ����Ѻ��ö��·ʹ�ҧ�ѹ�ء���Ẻ��������իտ �͡�ҡ��� �ѧ����á��¾ѹ�����չ GBA1 ���������§�Ѻ�ä�����㹼����� PD ����ҳ 5�10 �����繵�
�õչ��ſҫԹ٤�չ (aSyn) ���������ʴ����չ SNCA ������õչ����Ѻ�Դ�ͺ��ѡ㹡�������Ǣͧ���պʹ� ASyn ��е������ ATM serine/threonine kinase ������������ѭ�ҳ����������������¢ͧ���������ѡ �����鹷ҧ��ë�����������ͷ���������ͻ��·��������������ǡѹ
����кػѨ�������§��ҹ����Ǵ����������˵�������ͧ�ҡ���ͧ�ҡ�ä����ѡ���������������ǹҹ�֧˹�觷�����: 46 �Ѩ��´�ҹ����Ǵ����������ѧࡵ�ҡ����ش ���� ��������ʡѺ�Ҧ����ŧ��С�������ʡѺ����˹ѡ
�������ҧ��� ��������ʡѺ�Ҧ����ŧ �� ���Ҥ�͵ ���� ����� �������ૺ �����˵�˹�����ҡó� ��觺觪��֧��������ѹ��Ѻ���������鹢ͧ�ä����Թ�ѹ ��������§����������ҡ�����������ѹ�Ѻ������ MPTP
����˹ѡ������ѹ���� ���� ����ҹ�� ���� �С��� ��ͷ ���������� ���ᤴ����� 㹷ҧ��Ѻ�ѹ ����������ʴ��س���ѵ�㹡�û���ͧ�к�����ҷ
��û�Сͺ�ҧ������� ���� �ä�����ͷ��չ��� MPTP
����
��úҴ�纷����ͧ�ѧ����Ǣ�ͧ���ҧ�ҡ�Ѻ�Ѩ�������§ �͡�ҡ��� �����Ҩ�����Һ���˵ط�����ԧ ���ա�úѹ�֡�������秼��˹ѧ�դ�������Ǣ�ͧ�Ѻ�ä����Թ�ѹ �дѺ�ô���ԡ����ʹ������դ�������Ǣ�ͧ�Ѻ��������§���������� 㹢�з���õԴ���� Helicobacter pylori �Ҩ������ôٴ����ͧ�Һҧ��Դ�� ������ L-DOPA
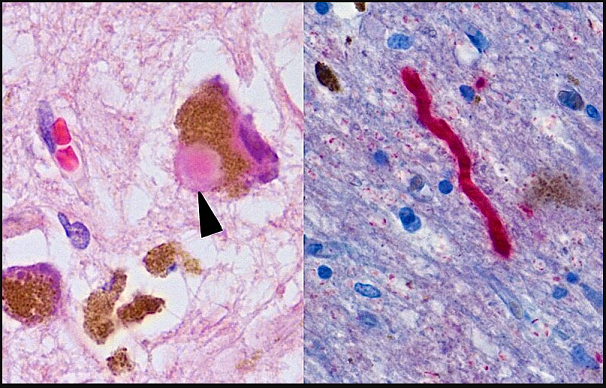
��������ʤ��ᾡ�ҷ���� Lewy body (����١��) ��й���õ� Lewy ����繺ǡ�ͧ��ſҫԹ�Ǥ�չ (���)
��Ҹ������Է��
�ѡɳзҧ��Ҹ��Է����ѡ��͡�õ�¢ͧ����ͧ�������ҷ���Ŵ�����ⴾ��չ���㹻�����ҷ�ҹ �������ҧ��觤�� pars compacta �ͧ substantia nigra ��� putamen �ҧ��ǹ�ͧ striatum �֧�Ѵ��ҧ��鹷ҧ nigrostriatal �ͧ�к� dopaminergic ����պ��ҷ�Ӥѭ㹡�äǺ�������������
������Ҥ����ҷ
��鹷ҧ��ѡ�����鹷ҧ�������ͻ�����ҷ�ҹ�Ѻ����dz��ͧ���� ���� ��鹷ҧ�ç ��鹷ҧ���� �����鹷ҧ�ç�Թ �����ǹ����ǹ˹�觢ͧ������-������ҷ�ҹ-�������-����Ԥ���ٻ
���
��ſҫԹ�Ǥ�չ (aSyn) ���õչ�������Ǣ�ͧ�Ѻ��â��觶ا�Թṻ�� ��â����������� ��С�û����������ͻ���ҷ � PD �õչ�Ҩ�١�ʴ��͡�ҡ�Թ� �Ѻ�Դ�ٻ ��С�͵���繡�����������͡�����ç���ҧ���� �����������ҷ �� ��ⵤ������й������� ��������ǹ��������Դ Lewy bodies �������Ǣ�ͧ�Ѻ��õ�¢ͧ�������ҷ��Ф����Դ���Ԣͧ������ͻ���ҷ
ǧ���غҷ��������Ǣ�ͧ�Ѻ����������ͧ�к�����ҷ����Ǣ�ͧ�Ѻ�������´�͡��പѹ ��ⵤ���� ��С�÷ӧҹ�ͧ�к�����ҷ���Ԥ����ѹ ���С���ѡ�ʺ ����Ҽ�ҭⴾ��չ��������ѡ��������� �觼�����дѺ�͡��ਹ���ͤ�տʻժ��� (ROS) �٧��� ����繾�ɵ��������з���������ԾԴ �õչ ������� ����������ҧ�����ⵤ�������Ѻ����������� ����������¢ͧ��ⵤ���¡�е�鹡�õͺʹͧ�ͧ�к�����ҷ�ѡ�ʺ��ҹ�ٻẺ���š�ŷ������Ǣ�ͧ�Ѻ����������� (DAMPs) �觼�������ҹԹ�ͧ�к�����ҷ�����ǡѹ ��д����˵ع�� �֧��е������Դ����ѡ�ʺ�ͧ�к�����ҷ��������¡�е����������
�����þⷫ�ʶ١�ʹ�����繡���Ӥѭ�ա��С��˹��㹡�ô��Թ�ͧ�ä �����ѡɳ��Ф�����������ͧ�ҡ���ԾԴ���������͡䫴���дѺ�٧
��õ�¢ͧ������ͧ
���˹�觷�������Դ��õ�¢ͧ������ͧ�Դ�ҡ��������õչ��ſҫԹ٤�չ����ִ�Դ�Ѻ�ٺԤ�ԵԹ�����������������ҧ�Դ���� �õչ����������¹�ӹ����������������������ҷ��С�͵����������������¡��� ���պʹ� ���պʹ�����ҹ���ҡ���鹤����á���ʹ�Ѻ���� ��������ͺ�ͧ�ҵ���о�չ������ ����������й���Ҩ������ҡ���������ҡ�÷ҧ�к����������������������� (�� �٭���¤�������ö㹡���Ѻ���������ҡ�ç�ǧ����͡�÷ӧҹ�ѵ��ѵԼԴ����) ������ä���Թ� ���պʹըоѲ�Ң�������մ� (substantia nigra) ����繺���dz�ͧ��ͧ��ǹ��ҧ�����ͧ��ǹ˹�� ����ش���¤���ͤ����� ����dz��ͧ����ҹ���繨ش��ѡ�ͧ����������ͧ�������ҷ��ä����Թ�ѹ �����պʹ��Ҩ����ͧ�������������� (���õչ���Դ���Ԩж١�ѡ�����ͻԴ������) �ٻẺ���� �ͧ��ſҫԹ٤�չ (�� ����������) �����������ǡѹ�����պʹ���й���õ������Ҩ���ٻẺ����繾�ɢͧ�õչ 㹼�������ä��ͧ������ �ѡ�����պʹ�㹺���dz���͡��ͧ ����»���ҷ�ѹ�ѹ��Ф�Һ��Ѥ���ª�� ������ѡɳ��Тͧ�ä��������� �ѡ�����¾� ���������¨���������ͧ������
������� ���� �����Դ���Ԣͧ�к��õ������������� ��С�÷ӧҹ�ͧ��ⵤ����Ŵŧ ��������ͧ�ҵ����������մ��ѡ�ѧࡵ�������Ѻ��������Ǣͧ�õչ �Ҩ����Ǣ�ͧ�Ѻ�������´�͡��പѹ ��������Ǣͧ�õչ ��С�õ�¢ͧ�������ҷ �����ѧ���Ѵਹ
�������ѹ�������ҧ�к�����ҷ������Ԥ����ѹ
�������ѹ�������ҧ�к�����ҷ������Ԥ����ѹ����ǹ����Ǣ�ͧ���ҧ�ҡ�Ѻ��Ҹ��Է�Ңͧ PD �к�����ҷ����ä���Ե�ҹ�ҹ���ͧ�ա������¹�ŧ�ҧ�ѹ�ء��������鹷ҧ���š�������ѹ �ä���Ե�ҹ�ҹ���ͧ�ҧ�ä�Ҩ������������§㹡���Դ PD ���ҡ�֧ 33% �ҡ����֡��˹�� �ä���Ե�ҹ�ҹ���ͧ���������§�Ѻ��������ʴ��͡�ͧ�õչ����䫵�������� T CD4+ ������§�Ѻ PD ��õԴ�����������������ö��е������Դ��ԡ��������Ԥ����ѹ�����ſҫԹ�Ǥ�չ ����Ҩ�Դ�ҡ������¹Ẻ���š�Ţͧ�õչ����� ��ſҫԹ�Ǥ�չ����ٻẺ����ͧ�ѹ ��觡��� Lewy bodies ����ö�Ѻ�Ѻ���������� ������������ö����Ш����ж١��е���ҡ�Թ�����ſҫԹ�Ǥ�չ���Ѻ�Ѻ����Ѻ MHC ���Թ�������� ������Դ��ûŴ�������䤹���������Դ����ѡ�ʺ �� IL-1β, IFNγ ��� TNFα
�������·��١��е�鹨��觼ŵ�͡�÷ӧҹ�ͧ�����䫵� ������¹���䷻��軡��ͧ�к�����ҷ����繿��䷻����繾�ɵ���к�����ҷ ���������䫵����ͧ������ç��˹�ҷ�軡��ͧ����������ͧ͢�������ҷ ��ä����Թ�ѹ ���������䫵��������ö����ͧ����������ͧ͢ⴾ��չ�����͵���� �������¹��ʹ����ਹ��ҹ MHC-I ��� MHC-II ������� T ���� T CD4+ ���١��е�鹴��¡�кǹ��ù�� ����ö��ҹ��ҹ������ʹ��ͧ (BBB) ��л������䤹���������Դ����ѡ�ʺ���ҡ��� �� �Թ�������-���� (IFNγ), TNFα ��� IL-1β �������������ʹ�ͧ������ʵ���С�ûŴ�������䤹���������Դ����ѡ�ʺ���������Ǣ�ͧ�Ѻ������µ�Ǣͧ BBB ��ä����Թ�ѹ �������Ԥ����ѹ�ա��Դ˹�觷������Ǣ�ͧ�Ѻ�ä����Թ�ѹ������䫵��ͺ�͡ ��о������մӢͧ�������ä����Թ�ѹ ���䫵�����ҹ������ö�����������¢ͧ����������ͧ͢ⴾ��չ���ҡ��� �͡�ҡ��� ���䫵����¡��ҡ�������ä����Թ�ѹ���ʴ��õչ�������Ǣ�ͧ�Ѻ�ä����Թ�ѹ��дѺ����٧���� ��� LRRK2 ��������º��º�Ѻ�����·��������ä����Թ�ѹ��ҹ��â�����ʹ���ʹ �͡�ҡ��� �дѺ��䤹���������Դ����ѡ�ʺ�٧ �� IL-6 �Ҩ�����Ѻ��Ե�õչ�����ͤ�տ ������õչ�ա��Դ˹�觷�辺������㹼������ä����Թ�ѹ ����Ҩ���������ѡ�ʺ�ͺ�͡��������ҡ���
����ѡ�ʺ�ͺ�͡�Ҩ�觼ŵ����ͧ-����� ����繺���dz�ͧ��ҧ��·������ǹ����Ǣ�ͧ���ҧ�ҡ�Ѻ�ä����Թ�ѹ �������ä����Թ�ѹ�ը��Թ�����������������¹�ŧ�����ջѭ�ҡѺ������˭����»ա������Դ�ѭ������ǡѺ���������� ��ſҫԹ٤�չ�١��Ե�������������Ҩ;¾��ҹ��鹻���ҷ�ǡ����ѧ��ҹ��ͧ �ҡ��鹨֧��ѧ����մ�
����ԹԨ���
�·���� ᾷ��л����Թ���ͧ��������»���ѵԷҧ���ᾷ����С�õ�Ǩ�ҧ�к�����ҷ �¨л����Թ�ҡ�÷ҧ�к����������� (���������Ǫ�� �ҡ����蹢�оѡ ���) ����ࡳ�����ԹԨ��·ҧ��Թԡ ��þ� Lewy bodies ���ͧ��ǹ��ҧ�ҡ��êѹ�ٵþ�ԡȾ�ѡ�������ѡ�ҹ�ش���·���ʴ���Ҽ��������ä����Թ�ѹ �ҡ�÷ҧ��Թԡ�ͧ�ä�Ҩᵡ��ҧ仨ҡ�ä����Թ�ѹ���������� ��觵�ͧ�ա�õ�Ǩ��ѹ�ҡ��������������ѹ�����١��ͧ�ͧ����ԹԨ���
�ä����Թ�ѹ�����ä������ѡɳФ���¡ѹ�Ҩ�Դ�����ҡ�������˵� �ä��ʹ���ʹ��ͧ �Һҧ��Դ �����þ���Ҩ������Դ "�ä����Թ�ѹ�ͧ" ��Ш��繵�ͧ���Ѻ��û����Թ������ҧ�������Ѻ����ѡ�� ��ͧ�Ԩ�ó�����¡�ä����Թ�ѹ�ǡ �� ����ҵ�˹����ͧẺ����˹����С�ý�ͧ͢�����к����ҧ������� �������������ѡ�������Ф����˹�Ңͧ�ä (�·���� ���ѡ���ä����Թ�ѹ�ѡ�ջ���Է���Ҿ���¡���㹡�äǺ����ҡ��㹡�����ҡ�þ���Թ�ѹ�ǡ) �ѵ�ҡ�ô��Թ�ä������Ǣ�� �����Դ���ԷҧʵԻѭ�����������������ͤ��������蹤��ͧ��ҷҧ �ҡ�������硹����������ҵ�㹪�ǧ��������Ҩ�觪��֧�ä����Թ�ѹ�ҡ���Ҩ��� PD �ͧ
ͧ��÷ҧ���ᾷ�������ҧࡳ�����ԹԨ������ͺ������з�����кǹ����ԹԨ������ҵðҹ ���������������鹢ͧ�ä ࡳ�����繷�����ѡ�ҡ����ش�Ҩҡ UK Queen Square Brain Bank for Neurological Disorders ��� U.S. National Institute of Neurological Disorders and Stroke ࡳ��ͧ Queen Square Brain Bank ��˹������������Ǫ�� (bradykinesia) �����Ѻ�ҡ����� �ҡ����蹢�оѡ ���ͤ��������蹤��ͧ��ҷҧ ���繵�ͧ�Ѵ���˵����� ��������ͧ�ҡ������ҹ���͡� 㹷���ش ��ͧ���ҡ��ʹѺʹع���ҧ���� 3 �ҡ�õ��仹��㹪�ǧ��������������Ѳ�ҡ��: ��������¢�ҧ���� �ҡ����蹢�оѡ ��ô��Թ�ä������� �ҡ�÷ҧ����������������ҵ� ��õͺʹͧ�������ⴻ����ҧ���� 5 �� ��ô��Թ�ä�ҧ��Թԡ���ҧ���� 10 �� ��С���Դ�ҡ��������ǼԴ���Է���Դ�ҡ����Ѻ��зҹ����ⴻ��ҡ�Թ� ��û����Թ��÷ӧҹ�ͧ�������������˹ѧ�����ù�俿����բͧ���˹ѧ�Ҩ�繻���ª��㹡���ԹԨ������мԴ���Ԣͧ�к�����ҷ�ѵ��ѵ�
����͵�Ǩ�ͺ����ԹԨ����ä����Թ�ѹ���¡�êѹ�ٵþ�ԡȾ ����Ҽ������Ǫҭ��ҹ�����Դ���Ԣͧ�����������դ��������������� 79.6% 㹡�û����Թ���ͧ�� ��� 83.9% ��ѧ�ҡ��Ѻ�觡���ԹԨ���㹡�õ�Ǩ�Դ����� ����͵�Ǩ�ͺ����ԹԨ��·ҧ��Թԡ�����¼����������繼������Ǫҭ����ѡ���¡�êѹ�ٵþ�ԡȾ ���������������¤�� 73.8% ��������� ����ԹԨ����ä����Թ�ѹ�դ�������� 80.6% ��С���ԹԨ�������ࡳ��ͧ Brain Bank �դ�������� 82.7%
��ö����Ҿ
��ö����Ҿ���¤��������� (CT) �ͧ�������ä����Թ�ѹ�ѡ���͡�һ���[98] ��ö����Ҿ���¤����������俿���դ���������ҡ���㹡���ԹԨ����ä��������Ҽ�ҹ� �������ҧ��觼�ҹ�ӴѺ��ö����Ҿ T2* ����ǵ�ҵ���������ӴѺ��ö����Ҿ����ǧ���˹ѡ�����Ƿ���������ͧʹ������������ҧ���� 3T ��觷���ͧ���ҧ�������ö�ʴ������繶֧���������ٻẺ��ö����ҾẺ '�ҧᩡ' ������ѡɳ��������մӷ�������ҹ��ѧ��ҹ��ҧ 㹡�����������ԧ����ҹ ���������ٻẺ���������դ������������Ш�����ä����ҡ ������������ԧ����ҹ����ҡ�ö����Ҿ���¤����������俿��Ẻ MRI �ͧ��������ҹԹ����ö�¡��м������ä����Թ�ѹ�ҡ�����»����� ��ö����Ҿ���¤����������俿��Ẻ MRI �ʴ������繶֧�ѡ��Ҿ㹡���¡��������ҧ�ä����Թ�ѹ��С�����ҡ�þ���Թ�ѹ�ǡ ����֧�����ҧ��������¢ͧ�к���������ͧ͢�ä����Թ�ѹ �����Ҥس���㹡���ԹԨ��¨��ѧ���������ҧ��õ�Ǩ�ͺ ��õ�Ǩ CT ��� MRI �������¡����ä���� ����Ҩ�����˵��ͧ�ͧ�ä����Թ�ѹ �����ǹ�˭��ѡ��������ͧ�ѡ�ʺ������ТҴ���ʹ������ѧ ��ʹ���ä��辺����� �� ���ͧ͡㹻�����ҷ�ҹ���������ͧ������
�Ԩ��������Ҽ�ҭ�ͧ�����ⴾ��չ㹻�����ҷ�ҹ����ö�Ѵ���µç���¡�õ�Ǩ�͡��������������Ẻ�����⾫Ե�����͡��������������Ẻ�����⿵����� ����ʴ�����������դ����ʹ���ͧ�٧�Ѻ����ԹԨ����ä����Թ�ѹ�ҧ��Թԡ �Ԩ�����������Ǣ�ͧ�Ѻⴾ��չ���Ŵŧ㹻�����ҷ�ҹ����ö�����¡����ä����Թ�ѹ����Դ�ҡ���� ��ä鹾�������������Ш��������ö���������ä����Թ�ѹ����ä����Թ�ѹ�ǡ ����Ѱ����ԡ� ����§ DaTSCAN ��ҹ�鹷�����Ѻ�����ѵԨҡ FDA �����¡����ä����Թ�ѹ���͡�����ҡ�þ���Թ�ѹ�ҡ�ҡ����蹡�еءẺ�ع�ç
��õ�Ǩ���¤����������俿�ҡ�����������㨴������ʹչ-123-����-�����ູ��š�ǹԴչ����ö�����кص��˹觢ͧ��éա�Ҵ�ͧ��鹻���ҷ�ͧ������������� �������ö�����ԹԨ����ä����Թ�ѹ��
����ԹԨ����¡�ä
����Թ�ѹ�ͧ � ����ö�¡���˵ص�ҧ� �ͧ����Թ�ѹ��ҡ����ѵ����ҧ�����´ ��õ�Ǩ��ҧ��� ��С�����ҧ�Ҿ���������� ������ҡ�þ���Թ�ѹ�ǡ���� �Ҩ���ҡ�á��������Ǥ���¡ѹ �����ҡ�÷������Ǣ�ͧ��ҡ���� �ҧ��ǹ���ҡ��Ẻ�Թ٤���;Ҹմ��� ������ͧ������Ẻ���պʹ�����Ǣ�ͧ�Ѻ�ҡ�÷ҧ�к����������� ����������ҡ�üԴ���Էҧ����Ѻ�����л���ҷ�������ҡ�÷ҧ�к����������� �ա�ҧ˹�� �ҡ��Ẻ��ŵԫ���Ϳ������ MSA �ѡ���ҡ�üԴ���Ԣͧ�к�����ҷ�ѵ��ѵ��������������� (�� �����ʵҫ��) ����Ҩ���ҡ�÷ҧ�к�����ҷ�ѵ��ѵ�����ѡ �ҡ�÷ҧ��ͧ��������ѡ �����ҡ�þ���Թ�ѹ����ѡ
������ҡ�þ���Թ�ѹ�ǡ���� ����Ǣ�ͧ�Ѻ�õչ��� �ҡ�����õչ��ſҫԹ٤���Թ ������� ����ҵ�˹��������Ẻ����˹�� (Progressive supranuclear palsy ���� PSP) ��С�����ҡ�ä����⤺ҫ�� (Corticobasal syndrome ���� CBS) PSP ����Ǣ�ͧ�Ѻ�ҡ����� ������� �ҡ�âͧ��ʹ���ʹ��ͧ ��С�è�ͧ�ͧ��ǵ�駨ӡѴ �Ҩ����Ǣ�ͧ�Ѻ�ҡ����ͧ��������ǹ˹����Т�Ѻ CBS ����Ǣ�ͧ�Ѻ����Թ�ѹẺ������ҵ� �ҡ����� ᢹ�ҼԴ���� ����ҡ�á�еءẺ�����Źԡ ����Ź�ͧ��ù��ʹ�����ҡ�÷������Ǣ�ͧ����ö�����¡����ᵡ��ҧ�����ҧ�����Դ���Ԣͧ���������Ƿ�����¡ѹ�Ѻ�ä����Թ�ѹ�������Һ���˵�
����Թ�ѹ�ҡ��ʹ���ʹ��ͻ�ҡ���ó�ͧ������ҡ�âͧ�ä����Թ�ѹ�����Ѻ��õ�Ǩ���˵ء�ó�ҧ��ʹ���ʹ (�� �ä��ʹ���ʹ��ͧ) ��÷������鹷ҧⴾ��չ�Ф���¤�֧�ѹ����˵آͧ����Թ�ѹ�ҡ��ʹ���ʹ��� PD �������Һ���˵� ��Ш֧���ҡ�ä���¡ѹ ����¡����ᵡ��ҧ����ö�����¡�õ�Ǩ�����§���ҧ�����´ ��û����Թ����ѵ� ��С�����ҧ�Ҿ
������ҡ�þ���Թ�ѹ�ǡ � �ä���ª�Դ�Ҩ�������ǹ˹�觢ͧ������ҡ�þ���Թ�ѹ�ǡ ���� ������ҡ�ä����⤺ҫ�� ��ý�������к� ����ҵ�˹����ͧẺ����˹�� ���������ͧ����������� Lewy bodies ����ԹԨ����¡�ä����ö�����»���ѵ����ҧ�����´��С�õ�Ǩ��ҧ��� (�������ҧ����鹷������������ҡ���е���ӴѺ) �����˹�Ңͧ�ä ��С�õͺʹͧ��͡���ѡ�� �ҡ���Ӥѭ�ҧ��С��:
������ҡ�ä����⤺ҫ�� � ���͵������ⴻ� ��еء��������� ��� �٭���¤�����ૹ���� ���á��� ��������·�������ͧ����
������ͧ����������� Lewy bodies � ���͵������ⴻ� ��������ö�ҧ�ѭ���˹�͡��ҡ����ҡ�÷ҧ���������� ����ҡ�÷ҧ�ѭ�ҷ��ѹ�ǹ (�Ҿ���ҧ��µ�������ͧ������ä���)
�ҡ�����Ẻ�ع�ç � �ҡ�ù���Ҩ�������ä����Թ�ѹ㹵�á ���ջѨ����Ӥѭ��������Դ����ᵡ��ҧ ��ҡ�����Ẻ�ع�ç �ҡ����蹨����ŧ������ա��������� (�բ��� PD) ���ҡ������ �ѡ����� ��Шо� DatSCAN �繻��� ��ý�������к� � ��ô��͵������ⴻ� �ء������ҧ�Ǵ���� ����������Ǣͧ�к�����ҷ�ѵ��ѵ� ���§���㨴ѧ�Դ���� �ҡ�úҺԹʡջ�ҡ� �ҡ������������ͧ���� ��мš�õ�Ǩ MRI ��
����ҵ�˹��������Ẻ�ء��� � ��ô��͵������ⴻ� ��è�ͧ�ͧ�ǵ�駷��ӡѴ �š�õ�Ǩ MRI �� ��Ф����ҡ�Ӻҡ㹷�ҷҧ����Դ����������ᵡ��ҧ�ѹ
�������� ����Ҩ���ҡ�ä���¡Ѻ PD ����:
�ä����ѡ�ʺ
�ä���µ���Ŵ�얨Ҥͺ
����������
�ҡ����秼Դ����
������ҡ�����/������·������Ǣ�ͧ�Ѻ�ѧ���͡��
������ͧ��������ǹ˹����о���Թ�ѹ���������§�Ѻ������ 17
�ä�ѹ�ԧ�ѹ
�������������㹻�����ҷ�ҹ������Һ���˵�
����������ͧ�к�����ҷ����ա�������ͧ�ҵ��������ͧ
������ͧ�����Өҡ�����ѹ����
���������蹪��
����Թ�ѹ�ҡ�ä�Ե���
�ä����ѹ
��û�ͧ�ѹ
����͡���ѧ������¡�ҧ���Ҩ����Ŵ��������§�ͧ�ä����Թ�ѹ������ѧ�� �ҡ����֡���Ԩ������ǡѺ����͡���ѧ������ͻ�ͧ�ѹ�ä����Թ�ѹ ����Ҽ�����͡���ѧ��»ҹ��ҧ�֧˹ѡ�դ�������§Ŵŧ 34% ��й����ѧ�֡�һ���ª�����Ҩ���Ѻ�ҡ����͡���ѧ���㹼������ä����Թ�ѹ
����չ�������Ъ��»���ͧ��ҧ����� ��Ŵ��������§���ҡ����ҡ��������ͧ��������դ���չ㹻���ҳ�ҡ��� �� ���
��õ�ҹ��������� �� �Ե��Թ������� ���Ѻ����ʹ�����ͧ�ѹ�ä��� ��š���֡���ѧ���Ѵ��駡ѹ �������ռ���ԧ�ǡ�����ҧ� �š���֡������ǡѺ��ѹ��Сô��ѹ�ѧ���Ѵ��駡ѹ ������ҵ�ҹ����ѡ�ʺ��������������´� (NSAIDs) ����Һ��͡��ͧ�������Ҩ���»���ͧ��ҧ����� ������������ԧ����ҹ㹻� 2010 ����� NSAID (�͡�˹�ͨҡ�����Թ) �դ�������Ǣ�ͧ�Ѻ���Ŵ�غѵԡ�ó����Դ�ä����Թ�ѹ���ҧ���� 15% (�٧����㹼����������������繻�Ш�) � �� 2019 ������������ԧ����ҹ�ѧ�������ö��ѹ����������§����� ����֡�����ª���ʴ������繶֧����������§�����ҧ������ͺ�����Ф�������§��͡���Դ�ä����Թ�ѹ���Ŵŧ
��èѴ���
�����Ҩ��դ���������㹡���Ԩ�����ҧ������ͧ ���ä����Թ�ѹ���ѧ������Ը��ѡ�ҷ���Һ��Ѵ �·���仼����¨����Ѻ��ô��Ŵ����Ƿҧͧ������������ҹ��û�Ѻ����¹�Զժ��Ե��ҡѺ����Ҿ�ӺѴ �Һҧ��Դ�Ҩ�����ͺ�����ҡ����л�Ѻ��ا�س�Ҿ���Ե�ͧ������ �ҷ������ä����Թ�ѹ���͡ķ����������дѺⴻ��չ���ҧ����������¹Ẻ�Ţͧⴻ��չ�����ͧ�ͧ�������µç ����ⴻ� (L-dopa) �ջ���Է���Ҿ�٧�ش㹡���ѡ���ҡ�÷ҧ�к����������� ����ѡ�������Ѻ����Ѻ���ⴻҴդ���͡����� (�� �����ⴻ�����ູ����䫴�) ������ ���� ����Ѻ��� COMT ��á�е��ⴻ��չ �������Ѻ��� MAO-B ���آͧ�������������������ä ����֧���Тͧ�ä�ѡ�Ъ��¡�˹���ҡ�����ҷ�����Ƕ֧��ҧ�鹡������ջ���Է���Ҿ�٧�ش
��������Тͧ�äẺ��ҡ�����дѺ�ͧ��Ҹ���Ҿ㹼������ä����Թ�ѹ�͡�� 6 ���� �������ѹ��Ѻ�ҡ�âͧ�ä������������ ���С�ҧ ������з��� ����ѡ��������á�ըش���������������Դ��������ŷ��շ���ش�����ҧ��äǺ����ҡ����мŢ�ҧ��§�ͧ�� ������ҧ�� ����������ⴻ�����й���Ҩ��Ҫ��ŧ����������ҵ�����᷹ �� �ҵ�ҹ MAO-B ����ҡ�е��ⴻ��չ ���ͧ�ҡ�դ�������§�٧�����Դ�����á�� ���ҧ�á��� �ҡ�ô�ʤ����·������Ǣ�ͧ�Ѻ����ⴻ��ѧ���դ�������ѹ�����ҧ�ҡ�Ѻ����������Ф����ع�ç�ͧ�ä�ҡ�����������ҡ���ѡ�Ҵ�������ⴻ� ��þԨ�óҤ�������§��л���ª��ͧ������������ѡ�����ҧ�ͺ�ͺ���������Ӥѭ���������Ѿ��ͧ�����´շ���ش ����С�ҧ�ͧ�ä����Թ�ѹ ���������ѡ��͡��Ŵ�ҡ�âͧ������ ��������Թ��Ҵ���͡����ش�ҡзѹ�ѹ��ͧ���Ѻ��èѴ������ҧ�ѹ��ǧ�� �ҡ�������� ��ü�ҵѴ (�� ��á�е����ͧ��ǹ�֡������ŵ�ҫ�ǹ�����դ���������٧) �������������չ�ҧ������ʹ����˹ѧ������蹹 �������ͧ����ⴻҷҧ�ҡ�Ҩ�繻���ª�� �ä����Թ�ѹ����з���� �������Դ������ҷ�·���ͧ���Ѻ����ѡ����ҡ�����ٻẺ ����֧�ҡ�÷ҧ�Ե�Ǫ�������Ы������� �����ѹ���Ե���������ء� �����Դ���Ԣͧ�����л������ �������������ö�Ҿ�ҧ�� ������ش���¢ͧ�ä ��ô���Ẻ��ФѺ��Фͧ���ͺ������ͻ�Ѻ��ا�س�Ҿ���Ե�ͧ������
��÷��ǹ Cochrane 㹻� 2020 ��辺��ѡ�ҹ�����Ѵ��ҡ�ý֡�ҧ�ѭ���ջ���ª���ͼ������ä����Թ�ѹ ��ͧ������ ���ͤ��������ͧ�ҧ�ѭ���дѺ��硹��� �š���֡�ҹ������ѡ�ҹ����դ�������Өҡ����֡�� 7 ����
�ѧ����ա���ѡ���ҵðҹ����Ѻ�����Ե��ѧ�ŷ������Ǣ�ͧ�Ѻ�ä����Թ�ѹ
��ô���Ẻ��ФѺ��Фͧ
������¢ͧ��ô���Ẻ��ФѺ��Фͧ��͡�û�Ѻ��ا�س�Ҿ���Ե�ͧ��駼�������Ф�ͺ���Ǵ��¡�ú�����ҡ����Ф������´�ҡ�ä ���ͧ�ҡ�ä����Թ�ѹ�������ö�ѡ�������¢Ҵ�� ����ѡ�Ҩ֧�鹷���ê��͡�������������С�û�Ѻ��ا�س�Ҿ���Ե �֧����繡���ѡ��Ẻ��ФѺ��Фͧ
��ô���Ẻ��ФѺ��Фͧ������Ѻ��ô��ŵ�������� ����Тͧ�ä �������Ǫҭ��ҹ��ô���Ẻ��ФѺ��Фͧ����ö���º�����ҡ�÷ҧ��� �Ѩ��·ҧ������ �� ����٭���¡�÷ӧҹ��С�çҹ ���Ы������� �������� ��Ф����ѧ������ǡѺ��ô�ç����
�͡�ҡ�������ʹѺʹع�ҧ���������駼�������Ф�ͺ�������� ��ô���Ẻ��ФѺ��Фͧ�ѧ������䢻ѭ�ҡ�ô��ż����´��� �����¾���Թ�ѹ�Ҩ��ͧ�Ѵ�Թ㨷���ҡ�Ӻҡ������ä���Թ� �� ��ͧ����������������� ������ͧ��������Ẻ����ҵѴ���͡����Ф� ��ͧ��������»����������ͻ����������������� ��������㴨֧����Ѻ��ô���Ẻ��ФѺ��Фͧ ����ҹ����Ẻ��ФѺ��Фͧ����ö���µͺ�Ӷ����������йӼ����¾���Թ�ѹ����ǡѺ��Ǣ�ͷ��Ѻ����зҧ����������ҹ�� ���ͪ����������µѴ�Թ����ִ�����ҹ���
��������������鹻���ҷ���Ǻ�����кǹ�������������Ҩ���Ѻ�š�з��ҡ�ä����Թ�ѹ ������Դ�ҡ�÷�ͧ�١��С����������������Ǫ�� (����к�¢ͧ�����͡�ҡ����������������ҹҹ) �й�����Ѻ��зҹ����÷���դس��ҷҧ����ҡ�äú��ǹ�����û����Թ����ҡ�������� ��Ф���͡Ẻ�������������������ա����§����٭���������������˹ѡ���Ŵ�ŷ�����Ңͧ�����Դ���Ԣͧ�к��ҧ�Թ����� ������ä���Թ� �Ҩ�Դ�ѭ��㹡�á� (dysphagia) ������������������㹡�ô��������С���Ѻ��зҹ�����㹷�ҵç�Ҩ�繻���ª�� ����ͧ�ԸըЪ���Ŵ��������§㹡�����ѡ�� ����ö�����Դ�ҡ������������µç����㹡������������
����ⴻ�����õչ���к���â������ǡѹ��������С�����ʹ-��ͧ �֧�觢ѹ�ѹ㹡����Ҷ֧����� ����Ѻ��зҹ�����ѹ���觼�������Է���Ҿ�ͧ��Ŵŧ �ѧ��� ����������������ⴻ� ��ú������õչ�ҡ�Թ仨֧������ҡ�Թ� ��Ф���Ѻ��зҹ�����������������¹��������᷹ ������ء��� �й�����Ѻ��зҹ��Ե�ѳ�������õչ��� �� ����ѧ���;�ʵ��������������˵ؼŷ�����¡ѹ ����Ŵ��ԡ����ҡѺ�õչ ����Ѻ��зҹ����ⴻ� 30 �ҷա������ 㹢�����ǡѹ ��èӡѴ����Ѻ��зҹ�õչ������������������§ ������Ѻ��зҹ�õչ����������
��þ�ҡó��ä
PD �ѡ�д��Թ仵������ �Ըա�û����Թ�����ع�ç������¡��� Unified Parkinson's disease rating scale (UPDRS) ����繵�Ǫ���Ѵ�����ѹ�����㹡���֡���Ԩ�·ҧ��Թԡ �͡�ҡ����ѧ�� MDS-UPDRS ����������ѹ���Ѵ�ŧ���� �Ըա���ѴẺ��ҷ�����¡��� Hoehn and Yahr scale (�վ��������á㹻� 1967) ����ҵ����ǹ������¡ѹ������¡��� Modified Hoehn and Yahr scale �١������ �ҵ����ǹ Hoehn and Yahr ��˹����о�鹰ҹ 5 ���Тͧ��ô��Թ�ä
�ҡ�÷ҧ�к������������Ҩ���Թ����ҧ�Ǵ���������������鹢ͧ�ä��Шд��Թ仪��ŧ������ѧ �ҡ������Ѻ����ѡ�� �����¨��٭���¤�������ö㹡���Թ���������ѧ�ҡ��ҹ�������� 8 �� ��е�ͧ��Դ��§��ѧ�ҡ��ҹ� 10 �� ������ҷ�����þ�ҡó��ä�ҧ�к����������Ǵբ�� 㹼�����Ѻ��зҹ����ⴻ� ���ҷ���ҡ�èд��Թ仨��֧���з���ͧ��觾Ҽ��������ҧ�ҡ�Ҩ�����ҹҹ���� 15 ��
�ա��Ժ�������ѹ��ô��Թ�ͧ�ä PD ���ᵡ��ҧ�ѹ�ͧ������: ��С���á��ͻ��������¢ͧ PD �����Թ����ҧ�Ǵ���� ������ѡɳ��Ф���ա�ô��Թ����ҧ�Ǵ���Ǣͧ�ҡ�÷ҧ�ѭ�� �Ե����ҷ ����к�����ҷ�ѵ��ѵ� �դ��������ͧ㹡���Թ�ҡ��� �ѵ�ҡ�����ª��Ե������� ��С���������ͧ�к�����ҷ������Ǣ�������մ� ��С�÷���ͧ ��ͻ��������¢ͧ PD �����Թ仪�� ���ա�ô��Թ�ͧ�ä�������ع�ç����ѵ�ҡ�����ª��Ե��ӡ���
��÷ӹ������ä�д��Թ����ҧ������кؤ�Ź��������ͧ�ҡ ���ط���ҡ��� �ҡ�� RBD ��������Ǣ�� ����֡�ҷ����ŧ ����ҡ�÷ҧ���������Ǣͧ PD ����������Ź���ŧ�դ�������ѹ��Ѻ��ô��Թ�ͧ�ä������Ǣ�� �ѵ�ҡ���������ͧ���������Ǩ��٧����㹼�����դ��������ͧ���¡���㹪�ǧ���ҷ�����Ѻ����ԹԨ��� 㹢�з����������ͧ�ҧʵԻѭ���Դ��鹺��¡���㹼�����������ҡ���� 70 ���������������ҡ��
���֧�� 2023 �ѧ����դ�������ѹ����Ѵਹ�����ҧ��ô��Թ�ͧ�ä PD ��Ф����ԡ�âͧ PD ����� ���ҧ�á��� �����ԡ�âͧ PD ������á�ѡ����Ǣ�ͧ�Ѻ�ҡ�÷ҧ�к���������������ѡ 㹢�з���������ѧ �ѡ����Ǣ�ͧ�Ѻ�ҡ�÷���������ǡѺ�к���������������ѡ �ա�úӺѴ�������ö��Ѻ��ا���ͺ�����ҡ������ҹ������дѺ˹�� ������ä���Թ� �����ԡ�è�����Ǣ�ͧ�Ѻ�ҡ�÷ҧ�к����������Ƿ���������ö�Ǻ���������� (�� ���Ӻҡ ���Ӻҡ ��лѭ��㹡���Թ���͡�÷ç���) ��������á������Դ�ҡ����ⴻ� ��觻�ҡ�㹼������ҡ�֧ 50% ��ѧ�ҡ������ⴻ������� 5 �� 㹷���ش ��ѧ�ҡ��ҹ� 10 �� ��������ǹ�˭��ѡ���ҡ�üԴ���Ԣͧ�к�����ҷ�ѵ��ѵ� �ѭ�ҡ�ù��Ѻ �������¹�ŧ�ҧ������ ��С����������¢ͧ��������ö㹡���Ѻ��� �ҡ������ҹ�� ���С����������¢ͧ��������ö㹡���Ѻ��� �з�����������ö㹡���Ѻ�������������ҧ�ҡ
���آ�¢ͧ������ PD Ŵŧ �ѵ�ҡ�����ª��Ե���������ҳ�ͧ��Ңͧ�����·��������Ѻ�š�з� �����������¢ͧ��������ö㹡���Ѻ������������ͧ������ ��ª���������������ä ���Тͧ�ä����ء����ҡ��� ����ջѭ��㹡�á� ��ǹ�繻Ѩ�������§��͡�����ª��Ե �ٻẺ�ͧ�ä������ѡɳ��蹤���ҡ���������ѡ ��觵ç�����Ѻ�ҡ������秷��� �ӹ������ѵ�ҡ���ʹ���Ե�дբ�� �ä�ʹ����ҡ������ѡ�����˵���ѡ�ͧ������ª��Ե ��о�����¡���㹼�����繾���Թ�ѹ�֧�ͧ����������º�Ѻ��Ъҡ÷����
㹻� 2016 �ä����Թ�ѹ������ռ�����ª��Ե�����š����ҳ 211,000 ��� ���������� 161% ������ 1990 �ѵ�ҡ�����ª��Ե������������ 19% �� 1.81 ��� 100,000 ��㹪�ǧ���Ҵѧ�����
��������ä����Թ�ѹ�դ�������§���ä��ͧ�������ҡ���һ�Ъҡ÷���件֧ 2 �֧ 6 ��� ��������ä����Թ�ѹ�٧�֧ 78% ���ä����Թ�ѹ������ä��ͧ������ �ä��ͧ����������Ǣ�ͧ�Ѻ�س�Ҿ���Ե���Ŵŧ㹼����¾���Թ�ѹ��м����� �ѵ�ҡ�����ª��Ե���������� ����͡�ʷ������¨е�ͧ���Ѻ��ô���㹺�ҹ�ѡ����Ҩ��٧���
�кҴ�Է��
�ä����Թ�ѹ���ä�к�����ҷ��������辺�������ѹ�Ѻ�ͧ����觼š�з���ͼ�餹�����š����ҳ 6 ��ҹ�� � �� 2021 �ä����Թ�ѹ���ä�к�����ҷ����������Ժ����Ƿ���ش��š���㹴�ҹ������ª��Ե����ѵ�ҡ���Դ�ä �Ѵ��ǹ㹻�Ъҡ�㹪�ǧ����˹�����������ҳ 0.3% 㹻�����ص��ˡ��� �ä����Թ�ѹ�������㹼���٧��������ѵ��������鹨ҡ 1% 㹡���������ҡ���� 60 ���� 4% �ͧ��Ъҡ÷���������ҡ���� 80 �� ��������¢ͧ�����������ä���������ҳ 60 �� �֧������ 5-10% �������㹪�ǧ���� 20 �֧ 50 �� ��觨Ѵ���ä����Թ�ѹ�����������ä����˹������ ��������Ѻ�š�з���ѵ����ǹ����ҳ 3:2 �������º�Ѻ���˭ԧ �ä����Թ�ѹ�Ҩ������¡���㹼��������������Ϳ�ԡѹ�������� (����֧����������) �����ҡ�ä鹾������繢������駡��� �ӹǹ����ԹԨ����ä����Թ�ѹ�����ͻ����������ҧ 8-18 ��� 100,000 ����ͻ�
�Ҵ��Ҩչ���ռ������ä����Թ�ѹ��ͺ����˹�觢ͧ��Ъҡ��š㹻� 2030 ��ФҴ��Ҩӹǹ�����¨���������繻���ҳ 14 ��ҹ��㹻� 2040 ��觡���Ժ�����¡��ҡ���кҴ�ͧ�ä����Թ�ѹ
�غѵԡ�ó�ͧ�ä��ͧ������������鹵������ ���������鹵���������Ңͧ�ä��дѺ�����¡���

Cr: Wikipedia, the free encyclopedia


TOP run up
| Create Date : 07 �ԧ�Ҥ� 2567 |
| Last Update : 7 �ԧ�Ҥ� 2567 16:33:02 �. |
|
1 comments
|
| Counter : 322 Pageviews. |
 |
|
|
��: �����   �ѹ���: 9 �ԧ�Ҥ� 2567 ����:7:04:45 �. �ѹ���: 9 �ԧ�Ҥ� 2567 ����:7:04:45 �. |
|
|
|
|
|
|
�
///
������Ҿ㹷ҧ��þٴ
�����������Ҿ㹡�÷����¼������"���¡�þٴ"
|
|
|
|
|
|
|
|
|

