|
|
|
การรักษามะเร็งปอดในระดับยีน
ในการรักษามะเร็งปอดชนิด small cell lung cancer (SCLC) ซึ่งเป็น systemic disease ที่มีการดำเนินโรคเร็วและสามารถกระจายไปที่อวัยวะสำคัญของร่างกาย เช่น สมอง และตับ ผู้ป่วยส่วนใหญ่จะมีชีวิตอยู่ได้เพียง 1-3 เดือน มีส่วนน้อยอยู่ได้นาน 6-12 เดือน การรักษา คือการใช้เคมีบำบัด ส่วนการรักษาด้วยการผ่าตัดและรังสีรักษาเป็นการรักษาเสริม ทั้งนี้ขึ้นกับการตอบสนองต่อการรักษาและสภาพของโรคในผู้ป่วยแต่ละราย จึงได้มีการศึกษาทางชีวโมเลกุลของมะเร็งปอดชนิด SCLC มากขึ้น ซึ่งพบว่ามีการขาดหายไปของ short arm ของ chromosome คู่ที่ 3 ซึ่งน่าจะมี tumor suppressor genes อยู่ในตำแหน่งที่ขาดหายไปของโครโมโซมนี้ การยับยั้งการทำหน้าที่ของยีนดังกล่าวเกิดขึ้นมากกว่ามะเร็งปอดชนิด non small cell lung cancer (NSCLC) มี oncogene c-myc ซึ่งมีความสำคัญต่อการเกิดมะเร็งปอดชนิด SCLC ผู้ป่วยส่วนใหญ่มีประวัติสูบบุหรี่จัด ตามปกติ oncogenes ในกลุ่มของ ras family เป็นยีนที่สำคัญในการควบคุมการเจริญของเซลล์ (Eagan et al. 1993; Rodenhuis et al., 1992) ทำให้ผู้ป่วยที่มี res mutation มีอัตราการรอดชีวิตต่ำในผู้ป่วย NSCLC ภายหลังจากการผ่าตัดแล้ว (Mitsudomi et al., 1991) ได้มีการศึกษาวิจัยโดยใช้ antisense ต่อ mutant K-ras oncogenes ในการรักษาผู้ป่วย NSCLC ในห้องปฏิบัติการ (Mukhopadhyay et al., 1991) พบว่าการยับยั้งการแสดงออกของ K-ras สามารถลดอัตราการเจริญของ H460a cells ได้โดยไม่ทำให้เซลล์นั้นตาย นอกจากนี้ได้มีการศึกษาวิจัยในห้องทดลองโดยใช้ retrovirus เป็นพาหะนำ express AS-K-ras (antisense-K-ras) เข้าไปในหนูซึ่งมี orthotopic human lung พบว่าสามารถหยุดการเจริญของ tumor ได้ (Gedges et al., 1993) ได้มีการศึกษาทดลองในผู้ป่วยที่มีการแพร่กระจายของมะเร็งไปยังปอดโดยให้ผู้ป่วยสูด IL-2 เข้าไปทางระบบทางเดินหายใจร่วมกับเคมีบำบัด พบว่าขนาดของมะเร็งที่มีการกระจายไปที่ปอดลดลงและไม่มีการแพร่กระจายของมะเร็งไปส่วนอื่นๆ ของร่างกายและอาการของผู้ป่วยดีขึ้น ดังแสดงในรูปที่ 4.1 (Alexander et al., 1999) เชื่อว่าในอนาคตจะมีการนำการรักษาด้วยยีนมาใช้ในการรักษามะเร็งโรคปอดมากขึ้น
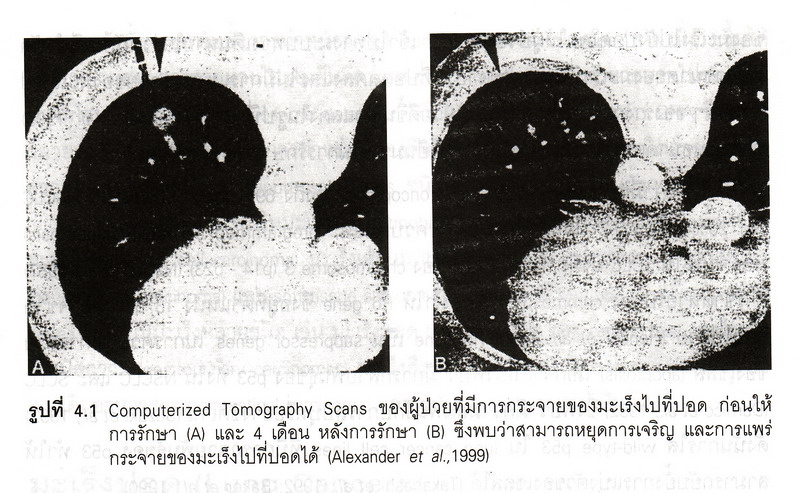
พบว่ามีการแสดงออกของ bcl-2 oncoprotein สูงถึง 69% ใน SCLC ส่วนใน NSCLC พบ 26% ซึ่ง bcl-2 มีผลต่อเซลล์ในการควบคุมและ programmed cell death (apoptosis) นอกจากนี้ใน SCLC ยังมีการขาดหายไปของ chromosome 3 (p14-p23) Naylor et al., 1987) การขาดหายไปของ chromosome 13q ทำให้ Rb gene เป็น suppressor genes ในการควบคุมการตายของเซลล์ (apoptosis) นอกจากนี้ยังพบว่ามีการกลายพันธุ์ของ p53 ทั้งใน NSCLC และ SCLC (Damico et al., 1992) ซึ่งพบว่ามีความสัมพันธ์กับการสูบบุหรี่อย่างชัดเจน (Suzuki et al., 1992) ดังนั้นการใส่ wild-type p53 ใน Lung cancer cell lines ที่มีการกลายพันธุ์ของ p53 ทำให้สามารถยับยั้งการแบ่งตัวของเซลล์ได้ (Takahashi et al., 1992; Baker et al., 1990)
โดยทั่วไปการรักษาผู้ป่วยมะเร็งปอดชนิด SCLC ด้วยเคมีบำบัดและรังสีรักษาจะได้ผลดี ผู้ป่วยมีชีวิตยืนยาวขึ้น หลักการรักษามะเร็งปอดชนิด SCLC คือ เคมีบำบัด ซึ่งมีการตอบสนองต่อการรักษาดีและมีพิษน้อยเมื่อให้ร่วมกับรังสีรักษา ความรู้เกี่ยวกับยีนที่ทำให้เกิดมะเร็ง (oncogenes) จะสามารถนำมาใช้ประโยชน์ใน human SCLC cell line ที่มีการแสดงออกของ L-myc gene จึงสามารถนำ L-myc antisense DNA มาใช้ในการยับยั้งการเพิ่มจำนวนของเซลล์มะเร็งในผู้ป่วย SCLC ได้ (Dosaka-Akita et al., 1995) ความรู้ทางชีวโมเลกุลของ SCLC ที่มีมากขึ้นจะช่วยในการค้นคว้าหาวิธีการรักษาที่ดีที่สุดสำหรับมะเร็งปอดชนิด SCLC ได้
ที่มา : รศ.ภก.ดร.จีระเดช มโนสร้อย, รศ.ภกญ.ดร.อรัญญา มโนสร้อย และ ศ.ภก.ดร.ยงยุทธ โรจนสกุล. การรักษาในระดับยีน. กรุงเทพมหานคร : โอเดียนสโตร์ : 2547.
| Create Date : 27 มกราคม 2551 | | |
| Last Update : 25 สิงหาคม 2552 10:45:45 น. |
| Counter : 2445 Pageviews. |
| |
|
 |
|
|
|
ความเจริญก้าวหน้าทางชีววิทยาโมเลกุล
โดย รศ . นพ . นรินทร์ วรวุฒิ
17 ม.ค.50
บทนำในระยะเวลา 50 ปีที่ผ่านมา ได้มีความพยายามศึกษาเพื่อค้นคว้าหาวิธีการรักษาโรคมะเร็งที่มีประสิทธิภาพให้ผู้ป่วยหายขาดจากโรคร้ายเหล่านี้ให้ได้มีการใช้การผ่าตัด การฉายแสง และการให้ยารักษาโรคมะเร็งซึ่งประสพความสำเร็จถึงระดับหนึ่ง
ความเจริญก้าวหน้าทางชีววิทยาโมเลกุล ได้ถูกนำมาประยุกต์ใช้เพื่อวิเคราะห์ในระดับโมเลกุล ถึงกลไกการเกิดมะเร็งจนสามารถค้นพบความผิดปกติที่เกิดขึ้นและเป็นสาเหตุของการเกิดโรคมะเร็ง ไม่ว่าจะเป็นการเปลี่ยนแปลงของปริมาณ DNA การเปลี่ยนโครงสร้างหรือจำนวนของโครโมโซม การกระตุ้นการทำงานของ Oncogenes หรือการยับยั้งการทำหน้าที่ปกติของ Tumor Suppressor Genes ทำให้เซลล์ปกติเกิดการเปลี่ยนแปลงหลายระยะจนกลายเป็น เซลล์มะเร็ง (Multistep Carcinogenesis) เกิดการเปลี่ยนแปลงเป็นขั้นตอนจากเซลล์ปกติ กลายเป็นเซลล์ระยะก่อนมะเร็ง (Premalignant Cells) และเปลี่ยนเป็นเซลล์มะเร็งในที่สุด (Malignant Transformation) จากการเปลี่ยนแปลงในระดับโมเลกุล ไปสู่การเปลี่ยนแปลงทางชีวเคมี จนเกิดการเปลี่ยนแปลงทางรูปร่างโครงสร้างและหน้าที่คุณสมบัติของเซลล์ มีทั้งการเจริญเติบโตที่ผิดปกติและการควบคุมการแบ่งตัวของเซลล์เสียไป (Growth and Proliferative Dysregulation) มีการเพิ่มจำนวนของเซลล์มะเร็งมากขึ้นจนเกิดเป็นก้อนมะเร็ง มีลักษณะของเซลล์ที่คล้าย Stem Cells เรียกว่า Dedifferentiation และมีความเป็นอมตะ (Immortalization) กล่าวคือ เซลล์ปกติจะมีอายุขัยจำกัด และตายไปด้วยขบวนการที่เรียกว่า Apoptosis หรือ Programmed Cell Death แต่เซลล์มะเร็งจะมีความผิดปกติของขบวนการดังกล่าว ทำให้เซลล์มะเร็งมีชีวิตอยู่ได้นานกว่าปกติ ผลลัพธ์ของการเพิ่มจำนวนและขนาดของเซลล์มะเร็ง มีคุณสมบัติที่คล้าย Stem Cells คือ มีการเจริญเติบโตแบ่งตัวได้ตลอดเวลา (Renewal Cells) และเซลล์สามารถดำรงชีวิตได้นานกว่าปกติ ทำให้ปริมาณเซลล์มะเร็งเพิ่มมากขึ้นผิดปกติจนเกิดเป็นก้อนมะเร็งซึ่งจะทำลายเนื้อเยื่อปกติข้างเคียง และแพร่กระจายไปสู่ส่วนต่าง ๆ ของร่างกาย (Metastasis) เกิดความผิดปกติทั้งทางกายภาพชีวภาพ และเมตตาโบลิค จนทำให้ผู้ป่วยด้วยโรคมะเร็ง ต้องเสียชีวิตในที่สุด
จะเห็นได้ว่ามะเร็งเป็นโรคที่เกิดจากความผิดปกติทางพันธุกรรม ดังนั้นข้อมูลที่ได้รับจากการศึกษาความผิดปกติที่เกิดกับเซลล์มะเร็งในระดับโมเลกุลทำให้ทราบถึงการเปลี่ยนแปลงจำเพาะที่เกิดขึ้น และสามารถประยุกต์ใช้ในการคิดค้นวิธีการรักษามะเร็งให้ตรงกับการเปลี่ยนแปลงของเซลล์ โดยไม่มีผลหรือมีผลน้อยต่อเซลล์ปกติของร่างกาย วิธีการหนึ่งที่สามารถนำมาใช้ได้คือ เมื่อทราบถึงการเปลี่ยนแปลงในระดับพันธุกรรมของเซลล์มะเร็งก็จะสามารถคิดค้นวิธีรักษา และแก้ไขความผิดปกติที่ระดับนั้น ๆ โดยตรง ซึ่งวิธีที่กำลังมีการศึกษาค้นคว้าวิจัยอยู่อย่างกว้างขวางทั่วโลกในขณะนี้คือ Gene Therapy การใช้วิธีการทางชีววิทยาโมเลกุลมาประยุกต์ ใช้ทางคลินิกดังกล่าว เพื่อแก้ไขความบกพร่องของเซลล์มะเร็ง ถือได้ว่า เป็นจุดหักเหที่สำคัญครั้งแรกในประวัติศาสตร์การแพทย์ของมนุษยชาติที่มีศักยภาพสูง ซึ่งอาจจะนำไปสู่การพิชิตโรคมะเร็งในที่สุด การรักษาดังกล่าวจะไม่ใช่การทำลายเซลล์มะเร็งแบบการรักษาเดิมที่เคยใช้อยู่ไม่ว่าจะเป็นการฉายแสงรังสี หรือการใช้ยาเคมีบำบัด หากแต่เป็นการยับยั้งหรือเปลี่ยนแปลงเซลล์มะเร็งเสียใหม่ในระดับพันธุกรรม ซึ่งเป็นการแก้ไขที่สาเหตุพื้นฐานของการเกิดโรคมะเร็ง
Gene Therapy เป็นความหวังใหม่ของแพทย์ที่จะเอาชนะโรคมะเร็งโดยอาศัยเทคโนโลยีทางพันธุวิศวกรรมศาสตร์ ซึ่งนอกเหนือจากการแก้ไขความผิดปกติของยีน ยังสามารถประยุกต์ใช้กับการรักษาโรคมะเร็งด้วยวิธีอื่น ๆ ได้ เช่น การใส่ยีนที่ทำให้เซลล์ปกติของไขกระดูกดื้อต่อยาเคมีบำบัด (Multidrug Resistance Gene) ทำให้สามารถให้เคมีบำบัดในขนาดสูงเพื่อทำลายเซลล์มะเร็ง โดยไม่มีผลเซลล์กระดูกปกติ การใส่ยีนเครื่องหมาย (Marker Gene) เข้าไปในเซลล์มะเร็งเพื่อติดตามการดำเนินโรค หรือการใส่ยีน Cytokines ชนิดต่าง ๆ เข้าไปในเซลล์ของระบบอิมมูนหรือเซลล์มะเร็งเพื่อเพิ่มภูมิต้านทานโรคมะเร็ง การใส่ยีนซ่อมแซม DNA ในเซลล์ปกติที่ถูกทำลายด้วยเคมีบำบัดที่ใช้ในการรักษาโรคมะเร็ง เช่น ยีน O-alkyl-guanine-DNA Alkyltransferase ซึ่งทำหน้าที่ซ่อมแซม DNA ที่ถูกทำลายโดยเคมีบำบัดกลุ่ม Nitrosourea ทำให้อาจป้องกันการเกิดมะเร็งเม็ดเลือดขาวที่เป็นผลแทรกซ้อนในระยะยาวจากการรักษาด้วยยากล่มดังกล่าว เป็นต้น จะเห็นได้ว่าบทบาทของ Gene Therapy มีมากมายกว้างขวางหลายวิธีที่จะนำมาใช้ในการรักษามะเร็งได้อย่างมีประสิทธิภาพต่อไป
Definition
Human Gene Therapy คือ วิธีการนำ Genetic Material ใส่เข้าไปในเซลล์ของผู้ป่วยเพื่อทำหน้า ท ี่ทดแทนยีนที่ขาดหายไป หรือทำหน้าที่ผิดปกติ หรือให้หน้าที่ใหม่สำหรับเซลล์นั้น ทำให้เกิดประโยชน์ทางการรักษาโรค ในระยะเวลา 30 ปีที่ผ่านมา ได้มีความก้าวหน้าทางวิทยาศาสตร์เป็นอย่างมากทางวิชาพันธุกรรม ชีวเคมี และ ชีววิทยาโมเลกุล ทำให้ทราบถึงการเปลี่ยนแปลงและความผิดปกติในระดับ
พันธุกรรมของโรคต่าง ๆ จนถึงขั้นนำความรู้เหล่านี้จากห้องปฏิบัติการมาให้ทางคลินิกในการรักษาผู้ป่วย
History of Gene Therapy
การใช้ Gene Therapy ในมนุษย์เริ่มครั้งแรกเมื่อวันที่ 22 พฤษภาคม ค . ศ . 1989 โดยเป็นการทดลองนำ Neomycin Resistance Gene มาใส่ในเซลล์ดังกล่าวเข้าไปในตัวของผู้ป่วย เพื่อการศึกษาถึงความเป็นไปได้ของเทคโนโลยีในการนำยีนจากภายนอกใส่เข้าไปในมนุษย์ และศึกษาถึงความปลอดภัยตลอดจนผลข้างเคียงที่อาจเกิดขึ้นจากวิธีการดังกล่าว เมื่อพบว่าเทคนิคในการนำยีนจากภายนอกใส่เข้าไปในเซลล์ของเม็ดเลือดได้ผลดี และอยู่ในร่างกายของมนุษย์ได้กว่า 100 วันติดต่อกัน เมื่อตรวจหายีนดังกล่าวโดยใช้เทคนิคของ Polymerase Chain Reacition จึงได้นำไปสู่การทดลองขั้นต่อไปคือ การนำ Gene Therapy มาใช้รักษาผู้ป่วย Adenosine Deaminase Deficiency ซึ่งเป็นโรคทางพันธุกรรมที่พบน้อย เกิดจากการขาดเอนไซม์ Adenosine Deaminase ซึ่งจำเป็นสำหรับการทำงานตามปกติ ของระบบอิมมูน การขาดเอนไซม์นี้ทำให้เกิดภาวะบกพร่องทางอิมมูนตั้งแต่เด็ก และเกิดการติดเชื้อได้บ่อยจนอาจมีอันตรายถึงชีวิตได้ จากความรู้ทางชีววิทยาโมเลกุลทำให้สามารถตรวจพบยีนที่สร้างเอนไซม์ชนิดนี้ และเข้าใจถึงกลไกการเกิดโรคจากความผิดปกติของยีนดังกล่าว การรักษาโรคนี้โดยใช้ Gene Therapy จึงเป็นวิธีรักษาโรคตามกลไกการเกิดโรค ดังนั้น เมื่อวันที่ 14 กันยายน ค . ศ . 1990 จึงได้มีการใช้ Gene Therapy มารักษาโรคนี้เป็นครั้งแรกโดยนำ Adenosine Deaminase (ADA) Gene มาสอดใส่ Retrovirus ซึ่งทำหน้าที่เป็นพาหะนำยีนดังกล่าวเข้าไปสู่เซลล์เม็ดเลือด Lymphocytes ของผู้ป่วยอายุ 4 ปี ซึ่งป่วยด้วยโรค Adenosine Deaminase Deficiency และเพาะเลี้ยงเซลล์ดังกล่าวในห้องทดลองโดยอาศัย T-Cell Growth Factor จนมีปริมาณมากพอจึงฉีดกลับเข้าไปในตัวผู้ป่วย การรักษาได้ผลดีผู้ป่วยมีระบบอิมมูนปกติหลังจากการได้รับยีน ADA ปริมาณเม็ดเลือด Lymphocytes ของผู้ป่วยหลังการรักษาเพิ่มปริมาณขึ้นถึงระดับปกติ และปริมาณโปรตีน ADA ใน T-Lymphocytes เพิ่มระดับขึ้นถึง 25 เปอร์เซ็นต์ ของปกติในผู้ป่วยที่ได้รับการรักษา และผู้ป่วยเริ่มมีปฏิกิริยาตอบสนองทางอิมมูนต่อตัวกระตุ้น
หลังจากนั้นก็ได้มีการศึกษาและวิจัยเรื่อง Gene Therapy ในการรักษาผู้ป่วยไม่ว่าจะเป็นโรคทางกรรมพันธุ์ เช่น Hemophilia, ADA-deficiency, Familial Hypercholesterolemia และโรคมะเร็งชนิดต่าง ๆ ได้แก่ Acute Lymphocytic Leukemia, Ovarian Cancer, Neuroblastoma
Methodology of Gene Therapy
วิธีการในการนำยีนใส่เข้าไปในเซลล์ที่ต้องการและทำหน้าที่ในเซลล์นั้นที่ใช้อยู่ในปัจจุบันนี้ ในการศึกษาวิจัยเรื่อง Gene Therapy มีอยู่หลายวิธีพอสรุปได้ดังนี้
- Physical Delivery Systems
- Calcium-phosphate Precipitation
- Electroporation
- Microinjection
- Protoplast Fusion
- Liposomal transfer
- Receptor-mediated Delivery
- Tissue Injection
- Viral-mediated Delivery Systems
- Retroviruses
- Adenovirus
- Herpes Simplex Virus
ปัญหาที่สำคัญที่เป็นข้อจำกัดในวิธีการต่าง ๆ ดังกล่าวข้างต้นในการนำยีนหรือ DNA ที่ต้องการใส่เข้าไปใน Mammalian Cells มี 2 ประการด้วยกันคือ
1. Low Effiency of Gene Expression ประสิทธิภาพในการสร้างโปรตีนของยีนใหม่ที่ใส่เข้าไปใน Mammalian Cells จะต่ำกว่าเมื่อใส่ใน Prokaryotic Cells มาก เช่น ในเซลล์ของมนุษย์จะมีส่วนของยีนใหม่สอดแทรกเข้าไปใน DNA ของเซลล์ในขนาดที่สั้นมาก เช่น ประมาณ 6 Kilobases มีผลทำให้เพียง 10-30 เปอร์เซ็นต์ ของเซลล์ที่พบว่ารับยีนใหม่เข้าไปและสามารถสร้างโปรตีนของยีนนั้นได้ จะมี Transciption Unit ที่สองที่อยู่ในรูปแบบที่สมบูรณ์ (Intact Form)
การพัฒนาประสิทธิภาพของ Gene Expression เมื่อใส่ยีนเข้าไปในเซลล์แล้วส่วนใหญ่จะเป็นเรื่องของการเลือกใช้ DNA ส่วนที่ควบคุม Expression ของยีนนั้น ๆ ให้เหมาะสม โดยเรียก Promoters ที่จะคุม Transcription ของยีนให้แรงพอที่จะกระตุ้นให้ยีนมีการสร้างโปรตีนในปริมาณที่มากพอในการทำหน้าที่ของยีนนั้น
2. Short-lived Response ระยะเวลาที่ยีนใหม่จะสร้างโปรตีน แม้ว่า Transfection ของยีนใหม่จะเกิดขึ้นสมบูรณ์แบบแล้วก็ตามมักจะสั้นเกินไป เช่น ระยะเวลาเป็นเดือนเท่านั้น ไม่ว่าจะใช้วิธีไหนก็ตามในการนำยีนใส่เข้าไปในเซลล์ ซึ่งสาเหตุอาจจะเกิดขึ้นจากการสอดแทรกเข้าไปในสายของโครโมโซม การกลายพันธุ์ (Mutation) Expression ของ Non-integrated DNA รวมทั้งการควบคุม Transcription ของยีน
เรื่องของ Reporter Gene System ก็มีความสำคัญกล่าวคือ การใช้ยีนที่เป็น Markers เพื่อตรวจสอบว่า การสอดแทรกของยีน (Insertion) ที่ใช้ในการทำ Gene Therapy มีประสิทธิภาพมากน้อยเพียงไรก็มีความสำคัญ และเป็นส่วนที่จะช่วยในการพัฒนาเทคนิคของ Gene Therapy และเพิ่มความสำคัญในการนำยีนจากภายนอกเซลล์ใส่เข้าไปในเซลล์
Routes of Gene Therapy
Gene Therapy สามารถนำมาให้ในผู้ป่วยได้หลายวิธี ขึ้นอยู่กับแหล่งของ Modified Cells ที่ใช้ดังต่อไปนี้
1. Gene Blockade สามารถนำ Tumor Suppressor Gene ซึ่งมีคุณสมบัติยับยั้งการเจริญเติบโตของเซลล์มะเร็งได้มาสอดใส่ใน Vector ที่เหมาะสม เช่น Retrovirus เป็น Gene Vector แล้วฉีดเข้าไปในร่างกายของผู้ป่วยโดยตรง
2. Stem Cell Therapy Retrovirus บางชนิดสามารถใช้เป็นพาหะ ในการนำยีนที่ต้องการใส่เข้าไปใน Stem Cells ของไขกระดูกโดยตรง แล้วใช้วิธีการของการเปลี่ยนไขกระดูก (Bone Marrow Transplantation) หรือนำ Retrovirus ซึ่งมียีนที่ใส่เข้าไปใหม่ฉีดเข้าไปในไขกระดูกโดยตรง ไวรัสดังกล่าวจะนำยีนที่ต้องการเข้าไปใน Stem Cell พร้อมกัน เช่น อาจนำ Multidrug Resistance Gene ใส่เข้าไปใน Retrovirus ซึ่งจะทำหน้าที่เป็นพาหะนำยีนนี้เข้าไปใน Bone Marrow Stem Cell ทำให้เซลล์ของไขกระดูกมีความทนทานต่อยาเคมีบำบัด สามารถให้ยาในขนาดที่สูงได้ เพื่อทำลายเซลล์มะเร็งได้มากขึ้น โดยไม่มีผลต่อเซลล์ของไขกระดูกที่มี Multidrug Resistance Gene อยู่ เป็นต้น
3. Receptor-linked Gene Transfer เป็นการนำยีนที่ต้องการใช้ในการรักษาโรคมาต่อเข้ากับโมเลกุลที่จับกับ Receptors ของเซลล์ที่ต้องการทำให้การที่ยีนที่ใช้ใน Gene Therapy ในการรักษาโรค Fat Metabolism
4. Inhalation-therapy สำหรับโรคของทางเดินหายใจส่วนต้น เช่น Cyctic Fibrosis อาจจะนำยีนที่ใช้รักษาใส่เข้าไปใน Adenovirus และให้ผู้ป่วยสูดดมพาหะดังกล่าวเข้าไปในปอดโดยตรง
5. Gene-injection อาจนำยีนของเชื้อโรคหรือเซลล์มะเร็งใส่เข้าไปในเม็ดเลือดและฉีดเข้าไปในตัวผู้ป่วย เพื่อกระตุ้นให้มีการสร้างภูมิต้านทานโรคที่จำเพาะสำหรับโรคนั้น อาจใส่ยีน Cytokine ร่วมด้วย เช่น Tumor Necrosis Factor เพิ่มขึ้น ทำให้มีการกระตุ้นระบบอิมมูนของร่างกายมากยิ่งขึ้น เป็นการนำเทคโนโลยีของ Gene Therapy มาใช้ในเรื่องของ Tumor Vaccine
6. Gene-medicines อาจนำยีนที่ต้องการ เชื่อมต่อกับ Carrier Substances บางชนิดทำให้สามารถเข้าไปในเซลล์ที่ต้องการได้ และฉีดเข้าไปที่อวัยวะที่ต้องการรักษาโดยตรง ตัวอย่างของการใช้ Gene Therapy วิธีนี้คือการรักษาโรค Duchenne Muscular Dystrophy
Potentiate Immunotherapy
การใช้ Gene Therapy มาประยุกต์ใช้กับ Cancer Immunotherapy คือ การเพิ่มการตอบสนองทางอิมมูนของเซลล์มะเร็งโดยตรง ซึ่งสามารถทำได้โดยการใส่ยีน Cytokines ชนิดต่าง ๆ เข้าไปในเซลล์มะเร็งโดยตรงหรืออาจจะใส่ยีน MHC Antigens เข้าไปในเซลล์มะเร็งทำให้เพิ่มการตอบสนองทางอิมมูนต่อเซลล์มะเร็งก็ได้ในการศึกษาระยะแรกในสัตว์ทดลอง ได้มีการนำยีน TNF และ IL-2 ใส่เข้าไปในเซลล์มะเร็งของหนูทดลอง พบว่าสามารถทำให้ก้อนมะเร็งของสัตว์ทดลองเล็กลงได้ ดังนั้นจึงมีการเตรียมการทำ Gene Therapy ด้วยวิธีดังกล่าวในคน คือ การป้องกันเซลล์ไขกระดูกด้วยการใส่ Multidrug Resistance (mdr) Gene ลงไปในเซลล์ตัวอ่อนของไขกระดูก (Hematopoietic Progenitor Cells) ก่อนให้ยาเคมีบำบัดขนาดที่สูง (Intensive chemotherapy) mdr-1 Gene ทำหน้าที่สร้างโปรตีนชื่อ p170 Glycoprotein ที่จะอยู่ที่บริเวณผนังของเซลล์ทำหน้าที่เหมือนเครื่องสูบน้ำและจะขับเคมีบำบัดจากภายในเซลล์ออกสู่ภายนอกเซลล์ (Efflux) ทำให้ระดับของยาภายในเซลล์ลดน้อยลง เกิดภาวะดื้อต่อยา และเนื่องจากยาหลายตัวถูกขับออกด้วยวิธีนี้ จึงทำให้เกิดการดื้อยาหลายชนิดจากสาเหตุเดียวกันเรียกเซลล์ที่มีการดื้อยาเคมีบำบัดแบบนี้ว่า Multidrug Resistance Phenotype การดื้อยาเคมีบำบัดด้วยวิธีนี้พบได้ในยาหลายชนิด เช่น Adriamycin, Vincristin, Vinblastine, Vindesine และ Taxol ในกรณีที่จะเปลี่ยนไขกระดูกอาจใส่ mdr Gene เข้าไปในเซลล์ของไขกระดูกปกติ เพื่อให้สามารถให้ยาเคมีบำบัดได้เต็มที่ในการใช้ยาครั้งต่อไป นอกจากนั้นเมื่อให้ยาเคมีบำบัดครั้งต่อไป เซลล์ปกติของไขกระดูกที่ไม่มี mdr Gene ที่ถูกทำลายไปคงเหลือแต่เซลล์ที่มี mdr Gene อยู่เท่านั้น ทำให้เมื่อมีการเพิ่มปริมาณของเซลล์ดังกล่าว ก็ยิ่งทำให้ไขกระดูกมีความคงทนต่อยาเคมีบำบัดมากยิ่งขึ้น และระยะเวลาที่ไขกระดูกจะฟื้นตัวจากผลของเคมีบำบัดจะเร็วมากยิ่งขึ้น
จะเห็นได้ว่าวิธีดังกล่าวจะเป็นการเพิ่มการตอบสนองของระบบอิมมูน ที่จำเพาะต่อเซลล์มะเร็งที่ตัดออกมาจากตัวผู้ป่วยโดยการใช้ยีน Cytokines เป็นตัวกระตุ้นและเป็นวิธีเลียนแบบการสร้างภูมิต้านทานโรคทางธรรมชาติ โดยอาศัยความรู้ทาง Molecular Bilogy Tumor Immunology และ Cell Biology ซึ่งอีกไม่นานผลการศึกษาดังกล่าวคงจะบอกได้ว่าวิธีดังกล่าวจะสามารถนำมาใช้ในการรักษาโรคมะเร็งอย่างมีประสิทธิภาพได้หรือไม่
Chemoprotection
ปัญหาสำคัญของการรักษาโรคมะเร็งด้วยเคมีบำบัดหรือรังสีรักษาคือผลข้างเคียงต่อเซลล์ปกติ ซึ่งจะจำกัดขนาดที่ใช้ในการรักษา (Dose-Limiting Toxicities) โดยเฉพาะต่อเซลล์ปกติที่มีการแบ่งตัวเร็ว
โดยเฉพาะผลข้างเคียงต่อ Stem Cells ในไขกระดูก วิธีการป้องกันผลข้างเคียงดังกล่าวที่ใช้อยู่ในปัจจุบัน
โดยไม่ต้องลดขนาดยาหรือรังสี
Antisense Oligonucleotides
วิธีหนึ่งของ Gene Therapy ในการรักษาโรคมะเร็งคือ การยับยั้งการทำงานของยีนที่เกี่ยวข้องกับการเกิดโรคมะเร็ง (Inhibition of Endogenous Gene Expression) ในปัจจุบันนี้วิธีที่ใช้อยู่อย่างแพร่หลายคือ การใช้ Antisense Oligonucleotides
Antisense Oligonucleotides คือ Oligonucleotides ซึ่ง Complimentary กับส่วนของ Messenger RNA ของยีนที่ต้องการจะยับยั้ง ดังนั้นจึงจับอย่างจำเพาะกับ mRNA เกิดเป็น DNA-RNA Hybrid เกิดขึ้นเดิม mRNA จะเป็นสายเดียวเมื่อจับกับ Antisense Oligonucleotides จะเกิดเป็นสายคู่เกิดขึ้น ซึ่งจะถูกทำลายโดย Rnase H ซึ่งเป็นเอนไซม์ที่ย่อยสายคู่ แต่ไม่ย่อยสายเดียวของ RNA นอกจากนี้ถ้า Antisense Oligonucleotide จับกับตำแหน่งที่เกี่ยวข้องกับการควบคุมการทำหน้าที่ของยีน เช่น บริเวณ Promotor และ Enhancer ก็จะยับยั้งการทำหน้าที่ของยีนนั้น ๆ ได้ เมื่อหน้าที่ของยีนถูกยับยั้งจะทำให้ไม่เกิดการสร้างโปรตีน ถ้าโปรตีนนั้น ๆ เกี่ยวข้องและจำเป็นสำหรับการดำรงชีวิตของเซลล์ ก็จะทำให้เซลล์นั้นตายได้ ดังนั้น Antisense Oligonucleotides จึงอาจสามารถใช้ในการรักษาโรคมะเร็งได้ เช่น การใช้ Antisense Oligonucleotides ที่จำเพาะกับ mRNA ของยีนมะเร็ง ที่เกี่ยวข้องกับการเจริญเติบโตที่ผิดปกติ (Autonomous Cell Growth) หรือคุณสมบัติอื่น ๆ ของเซลล์มะเร็งที่สำคัญของเซลล์มะเร็งตามต้องการ
Drug Targeting
วิธีการทาง Gene Therapy สามารถนำมาประยุกต์ใช้เพื่อเพิ่มความจำเพาะของยาเคมีบำบัดต่อเซลล์มะเร็งได้ โดยอาศัยหลักการที่ว่า พาหะที่ใช้ในการนำยีนเข้าสู่เซลล์จะ Express ในเซลล์ของเนื้อเยื่อบางชนิดหรือในเซลล์มะเร็ง แต่ไม่เกิดการทำหน้าที่ในเซลล์ทุกชนิด ซึ่งเกิดจากการที่มี Transcription Factor ที่ควบคุม Promoter ของยีนเฉพาะในเซลล์นั้น ๆ ดังนั้นถ้าเป็นเซลล์อื่น เช่น เซลล์ปกติที่ไม่มี Transcription Factor ต่อ Promoter ของพาหะที่ใช้อยู่ ก็จะไม่เกิดการทำหน้าที่ของยีนนั้น ๆ ดังนั้นเมื่อใช้ Promoter ที่เหมาะสมต่อกับยีนที่ต้องการให้ Express เช่น Alpha-fetoprotein Promoter ต่อกับยีนที่ใช้ ก็จะทำให้ Expression ของยีนนั้นเกิดขึ้นจำเพาะในปริมาณมากในเซลล์ที่มี Transcription Factors ที่ควบคุม Alpha-fetoprotein Promoter ที่มีประสิทธิภาพสูง เช่น ใน Hepatocellular Carcinoma ที่สร้าง Alpha-fetoprotein แต่จะมีผลน้อยต่อ Normal Adult Liver ซึ่งไม่สร้าง Alpha-fetoprotein ในขณะนั้นในทางกลับกันถ้าต้องการให้ยีนที่ใส่เข้าไปออกฤทธิ์ในตับปกติก็ทำได้โดยใช้ Promoter ที่ออกฤทธิ์ในตับปกติซึ่งจะควบคุมยีนที่ต้องการให้ Express เช่น เลือกใช้ Alpha-fetoprotein (AFP) Promoter เมื่อต้องการให้ HSV Gene Express ใน Hepatocellular Carcinoma Cell แต่ถ้าต้องการให้ HSV Gene Express ใน Normal Liver Cells ก็เลือกใช้ Albumin Promoter และถ้าใช้ยีนที่เป็นเอนไซม์ที่ทำหน้าที่เปลี่ยน Prodrug ให้กลายเป็น Active Chemotherapy ก็สามารถเหนี่ยวนำให้เกิดยาเคมีบำบัดที่มีความเข้มข้นสูงในเซลล์ที่ต้องการได้เรียกวิธีการนี้ว่า Virally Directed Enzyme Prodrug Therapy (VDEPT)
ตัวอย่างของการใช้เทคนิค VDEPT ในการทำให้ยาเคมีบำบัดมีความจำเพาะต่อเซลล์มะเร็ง อาจทำได้โดยนำยีน Cytosine Deaminase ซึ่งสร้างเอนไซม์ที่เปลี่ยนยา 5-Fluorocytosine (5-FC) ให้กลายเป็นยาเคมีบำบัด 5-Fluorouracil (5-FU) โดยใช้ Promoter ที่เหมาะสม เช่น จากการศึกษาพบว่ามะเร็ง Cholangiocarcinoma ซึ่งเป็นมะเร็งตับที่พบมากทางภาคตะวันออกเฉียงเหนือของประเทศไทย เกี่ยวข้องกับการเป็นพยาธิใบไม้ในตับ (Opisthorchis viverini) จากการกินตัวอ่อนของพยาธิในก้อยปลาซึ่งทำจากปลาน้ำจืดดิบ มะเร็งชนิดนี้มีระดับของ C-neu Oncogene สูงถึง 80 เปอร์เซ็นต์ ของผู้ป่วยที่ตรวจ ดังนั้น ในรายที่มีการสร้าง C-neu Oncoprotein มากอาจรักษาได้ด้วย Gene Therapy โดยการนำ Retroviral Vector ที่ประกอบด้วย C-neu Promoter ต่อกับยีน Cytosine Deaminase ใส่เข้าไปในเซลล์มะเร็งที่มีการสร้าง C-neu Oncoprotein ซึ่งจะมี Transcription Factor ที่ควบคุม C-neu Promoter อยู่ในขณะที่เซลล์ปกติไม่มี จึงเกิดการกระตุ้น ให้มีการสร้างเอนไซม์ Cytosine Deaminase มากขึ้น และเอนไซม์จะเปลี่ยน ยา
5-FC ซึ่งไม่มีพิษต่อร่างกายกลายเป็น 5-FU ซึ่งเป็นยาเคมีบำบัด มีฤทธิ์รักษาโรคมะเร็งได้ ซึ่งขบวนการนี้จะเกิดเฉพาะที่ในเซลล์มะเร็งที่มียีนดังกล่าวอยู่เท่านั้น ทำให้สามารถเพิ่มประสิทธิภาพและความจำเพาะของการรักษามะเร็งด้วยยาเคมีบำบัดได้
Gene Replacement Therapy
การเกิดมะเร็งเป็นผลของความผิดปกติในระดับพันธุกรรม เกี่ยวข้องกับความผิดปกติของโครโมโซม DNA Content, Oncogenes, Tumor Suppressor Gene, Growth Regulatory Genes และยีนที่เกี่ยวข้องกับการแพร่กระจายของโรค (Metastasis) ดังนั้นในกรณีของการขาดหาย (deletion) หรือไม่ทำหน้าที่ตามปกติของยีนหนึ่งเป็นสาเหตุของการเกิดโรคมะเร็ง หรือ การแพร่กระจายของโรค การใช้ Gene Therapy เพื่อให้ยีนที่ขาดหายไปนั้นกับเซลล์มะเร็ง หรือทำให้ยีนที่ผิดปกติทำหน้าที่ตามปกติ จึงเป็นวิธีหนึ่งในการรักษาโรคมะเร็งตามกลไกการเกิดโรคในระดับโมเลกุล การเกิดมะเร็งนอกจากจะเกิดจากการกระตุ้นการทำงานของ Oncogene ดังนั้นแนวทางในการใช้ Gene Therapy ในการรักษาคือ การยับยั้งการทำงานของยีนอีกกลุ่มหนึ่งที่ทำหน้าที่ปกติที่ก่อให้การเกิดมะเร็ง (Tumor Suppressor Genes) โดยสรุปการรักษาด้วย Gene Therapy จะเป็นการเติมยีนที่ขาดหายไปหรือไม่ทำงานให้เซลล์มะเร็ง เพื่อเปลี่ยนเซลล์มะเร็งให้กลายเป็นเซลล์ปกติ ยีนเหล่านี้พบน้อยกว่ายีนมะเร็งมากเท่าที่ตรวจพบขณะนี้ แสดงในตารางที่ 20.1

การยับยั้งหน้าที่ปกติของ Tumor Suppressor Gene เหล่านี้เกิดขึ้นได้หลายวิธี เช่น การขาดหายไปของยีนที่ตำแหน่งนั้น ๆ (Allele Loss) การขาดหายไปของส่วนของโครโมโซมที่ยีนนั้นอยู่ (Chromosome Deletions) หรือการเกิดการเปลี่ยนแปลงในระดับ DNA เกิด Mutation ทำให้การทำหน้าที่ของยีนนั้นผิดปกติไป ซึ่งตัวอย่างของการยับยั้งการทำหน้าที่ปกติของ Tumor Suppressor Genes สามารถอธิบายให้เข้าใจได้โดยใช้ข้อมูลจากการศึกษาในมะเร็ง Retinoblastoma ซึ่งเป็นมะเร็งตาที่พบมากที่สุดในเด็กเล็ก พบเป็นสาเหตุของการตายจากมะเร็งในเด็กประมาณ 1 เปอร์เซ็นต์ และเป็นมะเร็งตาที่พบมากที่สุดในเด็ก โดยที่ 40 เปอร์เซ็นต์ของผู้ป่วย มีประวัติในครอบครัว (Familial History of Retinoblastoma) ถ้าเป็นกลุ่มของผู้ป่วยที่มีประวัติในครอบครัวมักจะเป็นมะเร็งของตาทั้งสองข้าง (Bilateral Involvement) และอาจเป็นได้หลายตำแหน่ง (Multifocal Lesions) จากการศึกษาการเปลี่ยนแปลงของ Retinoblastoma Gene ซึ่งอาจเกิดที่ระดับโครโมโซม หรือ DNA ก็ได้
ลักษณะที่สำคัญที่ทำให้เกิดก้อนมะเร็งขึ้นคือ การเจริญเติบโตของเซลล์มะเร็ง ซึ่งยีนกลุ่มที่ทำให้เกิดการเจริญเติบโตอย่างรวดเร็วของเซลล์คือ ยีนมะเร็ง (Oncogenes) ในทางตรงข้ามจะมียีนอีกกลุ่มหนึ่ง
ทำหน้าที่ตรงกันข้ามยีนมะเร็ง โดยจะยับยั้งการเจริญเติบโตและการแบ่งตัวของเซลล์ (Tumor Suppressor Genes หรือ Anti-oncogenes) ซึ่งกลไกการยับยั้งการเจริญเติบโตของเซลล์ มีหลายลักษณะดังนี้
1. Transcription factors Tumor Supressor Genes บางชนิดทำหน้าที่เป็น Transcription Factor
ซึ่งจะควบคุมยีนที่ทำหน้าที่เกี่ยวกับการเจริญเติบโตของเซลล์ เช่น Retinoblastoma (RB1) และ p53 Tumor Suppressor Genes อาจจับกับ DNA และควบคุมการทำงานของยีนที่ควบคุมการเจริญเติบโตของเซลล์ ยีน CCAAT-Enhancer Binding (C/EBP) เป็นยีนซึ่งสร้างโปรตีนที่เป็น Transcription Factor ซึ่งจะยับยั้งการเพิ่มจำนวนของเซลล์
2. Negative Control on Oncogenes Neurofibromatosis (NF1) Tumor Suppressor Genes จะยับยั้งการทำงานของ RAS Oncogene
3. Apoptosis การควบคุมจำนวนของเซลล์ให้มีปริมาณที่เหมาะสมคือ การที่เซลล์แก่ตายไปตามอายุขัย ซึ่งเรียกว่า Apoptosis หรือ Programmed Cell Death ยีนที่ควบคุมการตายของเซลล์คือ p53 Tumor Suppressor Genes ส่วนยีนที่ทำหน้าที่ตรงกันข้ามคือ ยีนมะเร็งชื่อ BCL2 ที่จะป้องกันไม่ให้เซลล์ตาย ทำให้เพิ่มปริมาณของเซลล์ขึ้นผิดปกติในระหว่างการเกิดมะเร็ง
4. Growth Arrest ยีนชื่อ Growth-arrest-specific (GAS) Genes จะเพิ่มปริมาณของ mRNA ขึ้นสูงสุดในระยะที่เซลล์หยุดการเจริญเติบโตในระยะ Synthetic (S) Phase ของ Cell Cyle ยีนชื่อ Statin เมื่อเพิ่มปริมาณมากขึ้นจะยับยั้งเซลล์ (Growth Arrested) และทำให้เซลล์แก่ (Senescent) ตามที่แสดงในตารางที่ 20.2
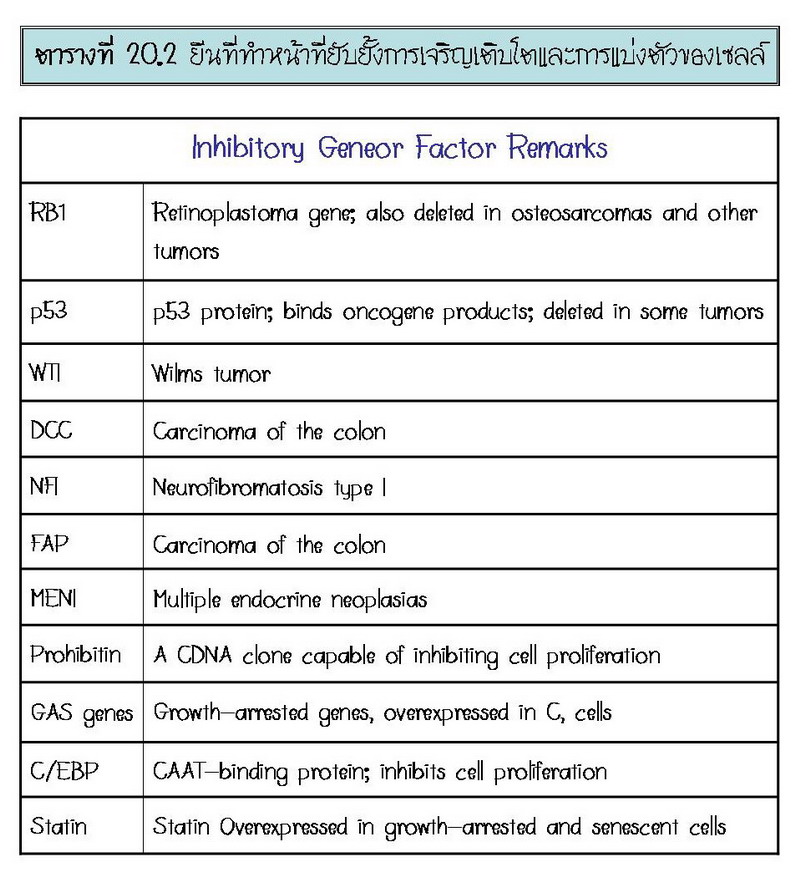
มะเร็งหลายชนิดอาจเกิดความผิดปกติของ Tumor Suppressor Genes ชนิดเดียวกันได้ เช่น การยับยั้งการทำงานของ Retinoblastoma Gene พบได้ในมะเร็งของตา (Retinoblastomas) มะเร็งกระดูก (Osteosarcomas) มะเร็งปอด (Small Cell Carcinoma) มะเร็งเต้านม (Breast Carcinomas) มะเร็งทางปัสสาวะ (Genitourinary Carcinoma) และ Soft Tissue Sarcomas การผิดปกติของ p53 Tumor Suppressor Genes พบได้ในมะเร็งหลายชนิด เช่น มะเร็งปอด (Non-Small Cell and Small Cell Lung Carcinomas) มะเร็งทางเดินปัสสาวะ (Genitourinary Carcinomas) มะเร็งศีรษะและคอ (Head and Neck Cancer) มะเร็งของทางเดินอาหาร (Gestrointestinal Carcinoma) และ Soft Tissue Sarcomas เป็นต้น
จากการศึกษาทางโครโมโซม (Cytogenetic Studies) พบว่า มีโครโมโซมที่ขาดหายไปในมะเร็งหลายชนิด เช่น มะเร็งปอดชนิด Small Cell Carcinoma มีการขาดหายไปของโครโมโซมคู่ที่ 3 (Chromosome 3 p Deletion) ซึ่งพบมากในมะเร็งชนิดนี้ชี้บ่งว่าน่าจะมี Tumor Suppressor Genes อยู่ที่ตำแหน่งที่ขาดหายไปของโครโมโซม และการยับยั้งการทำหน้าที่ของยีนดังกล่าวเรียกว่า Loss of Heter-ozygosity ซึ่งสามารถจะวิเคราะห์หาได้โดยใช้เทคนิคทางโครโมโซม และชีววิทยาโมเลกุล (Molecular Biology)
Molecular Vaccination
วิธีการหนึ่งของระบบอิมมูนในร่างกายที่ใช้ในการกำจัดเซลล์มะเร็ง คือ การที่ T Lymphocytes จับกับเซลล์มะเร็งโดยอาศัยการจับกับ T-cell Receptor และ Class I Histocompatibity Antigen (HLA) และ Intercellular Adhesive Molecules (ICAM) ซึ่งปฏิกิริยาทางอิมมูนเหล่านี้อาศัย Cytokines ในการเพิ่มปฏิกิริยาตอบสนอง ดังนั้นจึงสามารถอาศัยเทคโนโลยีทาง Gene Therapy ในการใส่ยีน Cytokine เข้าไปในเซลล์มะเร็ง หรือ T-cells เพื่อเพิ่มปฏิกิริยาตอบสนองต่ออิมมูนในการทำลายเซลล์มะเร็ง
ตัวอย่างของการใช้ Molecular Vaccination ที่มีการศึกษาอยู่ในปัจจุบันมีการใช้ยีน HLA B7 IL-2 IL-4 ใส่เข้าไปในเซลล์มะเร็ง แล้วฉีดเข้าไปในตัวผู้ป่วยเพื่อใช้เป็นวัคซีนในการกระตุ้นภูมิต้านทานต่อโรคมะเร็ง ดังแสดงในตารางที่ 20.3
วิธีการของ Molecular Vaccine ที่ใช้ในการรักษาโรคมะเร็งในปัจจุบันนี้จะเป็นการนำยีน Cytokine ที่ต้องการ เช่น IL-2 มาดัดแปลงและใส่เข้าไปมะเร็งที่แยกมาจากตัวผู้ป่วย เซลล์ที่ได้รับยีน IL-2 เข้าไปจะถูกฉีดกลับเข้าไปในตัวผู้ป่วยในลักษณะเดียวกับการฉีดวัคซีนทั่วไป และมักจะฉายแสงรังสีที่เซลล์มะเร็งนั้นเสียก่อน เพื่อทำให้เซลล์ไม่สามารถจะแบ่งตัวแพร่กระจายได้ต่อไปเมื่อฉีดเข้าไปในตัวผู้ป่วย เมื่อเซลล์ดังกล่าวถูกฉีดเข้าไปในตัวผู้ป่วยก็จะสร้าง IL-2 กระตุ้นให้ Accessory Immune Cell เข้ามาหาและสร้าง Cytokines ชนิดอื่น ๆ เช่น Interferon-gamma ซึ่งมีฤทธิ์ทำลายเซลล์มะเร็งได้ และยังกระตุ้นให้มีการสร้าง ICAM ที่ผิวของเซลล์มะเร็งซึ่งจำเป็นสำหรับการจับกับ T-Cell IL-2 ที่สร้างมาจากเซลล์ยังกระตุ้นการทำหน้าที่ T Lymphocytes ซึ่งจะเข้ามาทำลายเซลล์มะเร็ง เมื่อมีการกระตุ้นระบบอิมมูน โดยอาศัยวิธีของ Molecular Vaccination ดังกล่าวซึ่งจะจำเพาะต่อเซลล์มะเร็งที่ฉีดเข้าไปก็จะส่งผลโดยรวมเพิ่มการทำลายมะเร็ง ที่อยู่ในร่างกายของผู้ป่วยด้วย เหมือนกับการฉีดวัคซีนป้องกันโรคอื่น ๆ
Safety of Gene Therapy
การรักษาโรคของ gene therapy มีความปลอดภัยมากน้อยเพียงใดต่อตัวผู้ป่วยเองและสิ่งแวดล้อมเป็นไปได้หรือไม่ว่า ในการที่เราพยายามเปลี่ยนแปลงสิ่งมีชีวิตในระดับพันธุกรรมอาจจะก่อให้เกิดการกลายพันธุ์ เกิดโรคใหม่ ๆ ที่มีอันตราย เกิดผลข้างเคียงจากการรักษาที่เราไม่คาดคิดมาก่อน เกิดจากสิ่งมีชีวิตใหม่ที่มีอันตรายต่อสิ่งแวดล้อม เนื่องจากปกติแล้วกว่าจะเกิดการเปลี่ยนแปลงทางพันธุกรรมในธรรมชาติ ใช้เวลายาวนานในช่วงของวิวัฒนาการอาจเป็นเวลานับล้านปี ในขณะที่เทคโนโลยีทางชีววิทยาโมเลกุลสามารถที่จะสร้างหรือเปลี่ยนแปลง Genetic Materials ได้ในระยะเวลาอันสั้น ซึ่งการสร้างสิ่งต่าง ๆ เหล่านี้อาจจะไม่สอดคล้องกับธรรมชาติและระบบนิเวศน์วิทยา ตามที่ควรจะเป็นตามขั้นตอนของการวิวัฒนาการทางธรรมชาติเกิดความไม่สมดุลของธรรมชาติเกิดขึ้น เป็นที่น่ายินดีว่า ประสบการณ์ของการวิจัยเรื่อง Gene Therapy ที่ผ่านมาไม่พบผลข้างเคียงที่อันตรายไม่ว่าจะในสัตว์ทดลองที่นับได้ถึง 106 ปี ของอายุของลิงทั้งหมดที่ใช้ในการทดลอง ตลอดจน 23 ปีของอายุมนุษย์ทั้งหมดที่ได้รับการรักษาด้วย Retroviral-Mediated Gene Transfer และไม่พบว่าอุบัติการณ์ของการเกิดโรคมะเร็งเพิ่มมากขึ้นในผู้ป่วยที่รักษาด้วย Gene Therapy สำหรับพาหะที่ใช้ในการนำยีนที่ต้องการเข้าไปสู่เซลล์ซึ่งที่ใช้มากคือ Retrovirus โดยทางทฤษฎีแล้ว ไวรัสที่เกิดการกลายพันธุ์จากการทดลองทาง Gene Therapy ไม่ควรจะมีผลเสียต่อธรรมชาติและสิ่งแวดล้อม เนื่องจากไวรัสดังกล่าวถูกทำให้กลายเป็น Defective Virus ดังนั้นจึงไม่ควรจะมีอันตรายต่อมนุษย์หรือสิ่งมีชีวิตอื่น ๆ อย่างไรก็ตามมีรายงานจากสภาวิจัยแห่งชาติของประเทศ สหรัฐอเมริกาที่พบลิง 3 ตัวที่ใช้ในการทดลองเรื่อง Gene Therapy ในการเปลี่ยนไขกระดูกเกิดมะเร็งต่อมน้ำเหลือง (T-Cell Lymphama) และมีการปนเปื้อนของ Helper Retrovirus ดังนั้นการทดลองเรื่อง Gene Therapy จึงมีความจำเป็นมากที่จะต้องใช้พาหะที่เป็น Helper Virus Free Vector ในการทดลองทุกครั้ง
Medical Ethics
ถึงแม้ว่าปัจจุบันนี้เรื่อง Human Gene Therapy ยังไม่เป็นปัญหาทางจริยธรรม และด้านกฎหมาย เนื่องจากอยู่ในขั้นตอนของการศึกษาวิจัยโดยอยู่ภายใต้การควบคุมอย่างเข้มงวดของคณะกรรมการการวิจัยทางคลินิกและคณะกรรมการจริยธรรมในการทำงานวิจัยในมนุษย์ แต่ในอนาคตอันใกล้นี้ เมื่อมีการใช้ Gene Therapy อย่างแพร่หลายมากขึ้น โดยเฉพาะเมื่อเทคโนโลยีเหล่านี้ง่ายขึ้นและสะดวกมากขึ้น จำเป็นต้องมีการคำนึงถึงจริยธรรมทางการแพทย์และกฎหมายในการนำวิธีการรักษานี้มาใช้ในผู้ป่วย ในกรณีที่ใส่ยีนเข้าไปในเซลล์ปกติ Somatic Cells ไม่ใช่ Germ Lines จะมีปัญหาน้อยกว่าเพราะจะไม่มีผลต่อไปในขั้นลูกหลาน Gene Therapy ในกรณีนี้จะคล้ายคลึงกับการเปลี่ยนอวัยวะเท่านั้น แต่ถ้าจะเป็นของ Germ Line เช่น มีการฉีดยีนเข้าไปใน Fertilized Oocytes ของผู้ป่วยระยะเจริญพันธุ์ อาจมีผลต่อลูกที่เกิดได้ซึ่งอาจก่อให้เกิดการกลายพันธุ์ที่มีอันตรายและมีการถ่ายทอดทางกรรมพันธุ์ได้ ผลข้างเคียงที่เกิดขึ้นเหล่านี้จากการเปลี่ยน Genetic Information ไม่สามารถจะคาดคะเนได้ในขณะที่ทำ Gene Therapy แต่จะเกิดเป็นผลข้างเคียงระยะยาว ดังนั้นจึงควรจะมีการศึกษาเรื่องนี้อย่างรอบคอบในสัตว์ทดลอง ไม่ควรที่จะรีบร้อนนำมาใช้ในมนุษย์ ถ้ายังไม่มีความแน่ใจเพียงพอกับผลระยะยาวที่อาจจะเกิดขึ้น โดยเฉพาะเรื่อง Germ line Gene Therapy ที่อาจจะส่งผลไปสู่ลูกหลานของผู้ป่วยที่ยังไม่เกิดมา
บทสรุป
ความเข้าใจของการเกิดมะเร็งในระดับโมเลกุลทำให้ทราบถึงพยาธิกำเนิดของโรคมะเร็งว่า เป็นผลมาจากความผิดปกติทางพันธุกรรม ดังนั้นการที่เริ่มมีความเข้าใจถึงยีนต่าง ๆ ที่ควบคุมการเจริญเติบโตของเซลล์ (Growth Regulation) การพัฒนาของเซลล์ (Cellular Differentiation) และการตายของเซลล์ (Apoptosis) ตลอดจนการแพร่กระจายของเซลล์มะเร็ง (Metastasis) ทำให้สามารถพัฒนาวิธีการรักษามะเร็งตามพยาธิกำเนิดของโรค ไม่ว่าจะเป็นเรื่องของ Gene Therapy เพื่อเปลี่ยนทดแทนหรือให้หน้าที่ใหม่ต่อเซลล์ด้วยการใส่ยีนเข้าไปในเซลล์ รวมไปถึงการพัฒนาทางเภสัชวิทยา เพื่อคิดค้นยาใหม่ ๆ ที่มีผลต่อขบวนการต่าง ๆ ของการเกิดมะเร็งในระดับชีวเคมีที่เกิดขึ้น โดยเป็นผลสืบเนื่องมาจากความผิดปกติทางกรรมพันธุ์ของการเกิดโรคมะเร็ง Gene Therapy จึงเป็นวิธีการรักษาโรคมะเร็งแบบใหม่ที่มีการนำมาใช้กับผู้ป่วยโรคมะเร็ง ในระดับงานวิจัยทางคลินิก จนกว่าจะทราบถึงผลการรักษาที่แน่นอนและผลข้างเคียงทั้งระยะสั้นและระยะยาว จากการศึกษาในห้องปฏิบัติการ (Preclinical Study) และการศึกษาถึงผลงานทางคลินิกในระยะต่าง ๆ ตั้งแต่ Phase I เพื่อทราบถึงขนาดของยาสูงสุดที่ผู้ป่วยรับได้ (Maximum Tolerated Dose) และผลข้างเคียงของการรักษา ซึ่งขนาดของยาหรือวิธีการที่ใช้จะนำไปใช้ในการวิจัยขั้นที่สอง (Phase II) คือ การศึกษาถึงประสิทธิภาพของการรักษา และ Phase III เป็นการเปรียบเทียบการรักษาแบบใหม่กับวิธีการรักษามาตรฐานที่ใช้อยู่ในปัจจุบัน ก่อนที่จะมีการนำเทคโนโลยีเหล่านี้มาใช้ต่อไปในอนาคต
ที่มา //w3.chula.ac.th/college/ahs/Leukemia_2006/chap_20.htm
| Create Date : 05 มกราคม 2551 | | |
| Last Update : 15 มกราคม 2552 8:32:29 น. |
| Counter : 4612 Pageviews. |
| |
|
| |
|
|
|
|
|

blog counterDiseño Web
Share on Facebook


ทาน ศีล ภาวนา ธรรมทั้ง 3 นี้
เป็นรากแก้วของความเป็นมนุษย์
และเป็นรากเหง้าของพระศาสนา
หลวงปู่มั่น ภูริทัตโต
ถ้าเรารู้เรื่องธรรมดาของโลก และรู้จักความเป็นจริงของธรรมแล้ว
เราก็จะไม่ต้องมีความยุ่งยากในการเป็นอยู่
เรื่องภายนอกนั้น ถึงเราจะศึกษาให้มีความรู้สักเท่าไรๆ
ก็ไม่ทำให้เราพ้นจากทุกข์ได้
สู้การเรียนรู้จิตใจของตนอยู่ภายในวงแคบๆ นี้ไม่ได้
ท่านพ่อลี ธมฺมธโร
อย่าไปอยากรู้เรื่องของคนอื่นมันเป็นทุกข์
ให้สนใจเรื่องของตัวเอง
คือเรื่องของกายกับใจ
ดูให้มันชัด
หลวงปู่เพียร วิริโย
สิ่งใดมันล่วงไปแล้ว สิ่งนั้นมันก็ล่วงไปแล้ว หมดไปแล้ว
ไม่ควรเอามาคิด มาติดอยู่ในใจ ละทิ้งให้หมด
ส่วนว่าอารมณ์อันเป็นอนาคตกาล
ดีร้ายประการใด ทั้งทางโลก และทางธรรม
สิ่งนั้นก็ยังอยู่ข้างหน้า คือยังไม่มาถึง
เวลาปัจจุบัน คือ เป็นเวลาเรานั่งภาวนา ฟังธรรม
สงบกาย สงบวาจา สงบจิต สงบใจ อยู่นี้แหละ
เป็นธรรมะปัจจุบัน ให้ระลึกภาวนาทุกลมหายใจเข้าออก...
หลวงปู่สิม พุทธาจาโร
... ให้รักษาศีล
ให้รู้จักพิจารณา เกิด แก่ เจ็บ ตาย
รู้จักแก้ไขจิตของตน ...
หลวงปู่จาม มหาปุณฺโญ
หลวงพ่อชา สุภทฺโท : ปล่อยวาง 1
พระอาจารย์สิงห์ทอง ธมฺมวโร : ธรรมสู่ใจ
หลวงปู่เหรียญ วรลาโภ : ไม่ยอมละ
ดาวน์โหลดหนังสือธรรมะ (Download E-Book) :


































ดาวน์โหลดหนังสือธรรมะ โครงการบูรพาจารย์ (Download E-Book) :












ดาวน์โหลดหนังสือวิธีปฏิบัติสมาธิ วิปัสสนากัมมัฏฐาน (Download E-Book) :




ดาวน์โหลดหนังสือธรรมะ สำหรับผู้ป่วย, ญาติ และผู้รักษา (Download E-Book) :





ดาวน์โหลดหนังสือพระไตรปิฎก :

ดาวน์โหลดหนังสือธรรมะทั่วไป (Download E-Book) :






 
ดาวน์โหลด (Download): วารสาร นิตยสาร และสถิติ ที่เกี่ยวข้องกับมะเร็ง:



ดาวน์โหลด (Download): เอกสาร, คู่มือมะเร็ง และที่เกี่ยวข้อง:




 

ลิงค์ (Link): เรื่องที่น่าสนใจเกี่ยวกับมะเร็ง



ลิงค์ (Link): การแพทย์ทางเลือก, การแพทย์แผนไทย และธรรมชาติบำบัด




Link: ลิงค์ หน่วยงาน, สถาบัน, องค์กร และที่เกี่ยวข้องกับมะเร็ง










Link: ลิงค์ หน่วยงาน, สถาบัน, องค์กรด้านการสาธารณสุข และที่เกี่ยวข้อง












ดาวน์โหลด (Download): กฎหมาย, ประกาศ, ระเบียบ, ข้อบังคับ, คำสั่ง







ดาวน์โหลด (Download): เอกสารข้อมูลทางการแพทย์และสาธารณสุขที่สำคัญ



ลิงค์ (Link): การเดินทาง, แผนที่, ตารางเวลา และการส่งกลับทางอากาศ :


















ลิงค์ (Link): หมายเลขโทรศัพท์, การติดต่อสื่อสาร และการขนส่ง







ลิงค์ (Link): ค้นหาแผนที่










สมาทานศีล 5
หลวงพ่อชา สมาทานศีล 5
พุทธมนต์, พุทธคุณ ๑๐๘ นำสวดโดย หลวงพ่อจรัญ ธิตธมฺโม
ทำวัตรเช้า นำสวดโดย หลวงพ่อจรัญ ธิตธมฺโม
ทำวัตรเย็น นำสวดโดย หลวงพ่อจรัญ ธิตธมฺโม
ทำวัตรเย็น นำสวดโดย หลวงพ่ออุทัย สิริธโร
พาหุงมหากา นำสวดโดย หลวงพ่อจรัญ ธิตธมฺโม
บทสวดพระคาถาชินบัญชร
บทสวดยอดพระกัณฑ์ไตรปิฎก
บทสวดโพชฌังคปริตร
พระคาถาสักกัตวา
หลวงพ่อชา สอนการทำสมาธิ
หลวงพ่อจรัญสอนกรรมฐาน ตอนที่ 3/9
หลวงพ่อจรัญสอนกรรมฐาน ตอนที่ 4/9
หลวงพ่อฤๅษี ลิงดำ สอนกรรมฐาน 40 ตอนที่ 1
หลวงพ่อฤๅษี ลิงดำ สอนกรรมฐาน 40 ตอนที่ 2
หลวงพ่อฤๅษี ลิงดำ สอนกรรมฐาน 40 ตอนที่ 3
หลวงพ่อฤๅษี ลิงดำ สอนกรรมฐาน 40 ตอนที่ 4
หลวงพ่อพุธ ฐานิโย สอนกรรมฐาน
ลิงค์ (Link): ข่าวสาร, ข้อมูล, บทความเกี่ยวกับน้ำท่วม
















ดาวน์โหลด (Download): เอกสาร คู่มือเกี่ยวกับน้ำท่วม












หมายเลขโทรศัพท์ที่สำคัญ :
  
  
  










Ayutthaya Thai Flood 2011
น้ำท่วมกรุงเทพ ปี 2485 (Bangkok floods in 1942)
Nuidears Flood Control
mobile flood barrier
ถุงคลุมรถ
ข้อควรปฏิบัติขับรถช่วงน้ำท่วม
Thai PBS ฝ่าวิกฤตน้ำท่วม พบหมอรถ 1/5 (23 ต.ค.54
Thai PBS ฝ่าวิกฤตน้ำท่วม พบหมอรถ 2/5 (23 ต.ค.54
Thai PBS ฝ่าวิกฤตน้ำท่วม พบหมอรถ 3/5 (23 ต.ค.54)
Thai PBS ฝ่าวิกฤตน้ำท่วม พบหมอรถ 4/5 (23 ต.ค.54)
Thai PBS ฝ่าวิกฤตน้ำท่วม พบหมอรถ 5/5 (23 ต.ค.54)
Thai PBS ฝ่าวิกฤตน้ำท่วม - พบหมอบ้าน 1/6 (22 ต.ค.54)
เพลง ประสบทุกข์ ประสบภัย ฝ่าไปด้วยกัน (ขับร้องโดย พนักงานไทยพีบีเอส
เพลงน้ำใจไทย (ขับร้องโดย แอ๊ด คาราบาว)
|
|
|
|
|
|
|
|
| |
|
|